Estado especial de la materia: helio superfluido

A través de la mejora de las técnicas, los investigadores tuvieron la oportunidad de trabajar a altas temperaturas y encontraron un estado iónico que dio lugar al segundo estado gaseoso llamado plasma. A continuación, los astrónomos, junto con el descubrimiento de las estrellas de neutrón, dieron lugar a un segundo estado sólido denominado materia hiperdensa. La capacidad de trabajar a temperaturas muy bajas dio lugar al segundo estado líquido, denominado estado superfluido. Él desafía las leyes más consistentes del estado líquido, cuya interpretación, incluso a nivel atómico, es muy difícil y discutida.
En este pequeño trabajo hablaremos del estado superfluido del helio, el superfluido más raro que han encontrado los físicos.
Características del helio
Fue descubierto por los astrónomos en el sol y posteriormente fue identificado entre los gases más escasos de la atmósfera. El helio que se puede encontrar en la atmósfera es principalmente 4 2 He, estando el isótopo 3 2 He en un porcentaje de 10-7%.
En 1.868 se descubrió el helio en la atmósfera del sol gracias al espectoógrafo. Se pudo conseguir calentando determinados minerales en la tierra. Hasta la explotación de los yacimientos de gas natural, la producción de helio era muy reducida, pero suficiente para las necesidades de laboratorio.
A nivel atómico, aunque la del helio tras el hidrógeno es muy simple (dos protones, dos neutrones, dos electrones), como hemos dicho antes, es el superfluido que adopta la conducta más rara.
Helio superfluido
Hacia 1900 los investigadores comenzaron a licuar todos los gases conocidos.
Como es sabido, cualquier gas puede ser licuado y solidificado en condiciones adecuadas por enfriamiento hasta una temperatura determinada. Y más aún, cuanto mayor es la presión sobre el gas, mayor es la temperatura de licuefacción. Por ejemplo, el propano y el butano pueden estar licuados por simple compresión en una botella a temperatura ambiente. Por tanto, en la licuefacción de un gas podemos aprovechar tanto la presión como la temperatura para conseguir nuestro objetivo.
A pesar de trabajar a muy baja presión en la práctica, la licuefacción de la mayoría de los gases requiere temperaturas muy bajas, con un límite de cero absoluto (-273,16°C = OK). En efecto, el oxígeno a presión atmosférica requiere una temperatura de -218°C, el nitrógeno -210°C, el cloro -101°C y el neón -248°C. A pesar de la dificultad que supuso la licuefacción de otros gases, con el tiempo y sobre todo debido a los avances de la técnica, se fue obteniendo la licuefacción de todos los gases. Uno de los gases que presentaba esta dificultad era el hidrógeno, cuya temperatura de licuefacción (-260°C) es muy baja. Por lo tanto, la temperatura de licuefacción del hidrógeno, muy próxima al cero absoluto, dificultó enormemente a los investigadores, obteniendo James Dewar en 1892.
Como todos sabemos, cuando las moléculas están estancadas (es decir, cuando no hay movimiento molecular), la energía cinética y por tanto la temperatura toman el valor cero. En el cero absoluto no hay movimiento molecular. Por lo tanto, ninguna molécula puede alcanzar un estado cero absoluto.
Así pues, como hemos dicho al principio de este pequeño trabajo, nos situaremos en el helio. En 1900 todos los gases, excepto el helio, fueron licuados. Aunque se trabajaron todas las vías de licuefacción del helio, por un lado, no se podía licuar y mucho menos solidificar, y por otro, los investigadores que lo hicieron pensaron que sólo podía estar en estado gaseoso, independientemente de su valor de presión y temperatura.
De hecho, la primera afirmación es correcta, ya que sólo por refrigeración el helio no puede solidificarse. Y en cuanto a la segunda afirmación, hay que decir que no es un gas sostenible, pero sí el más difícil de liquidar. La licuefacción del helio la obtuvo el físico holandés Kammerling Onnes en 1908. Por lo tanto, todos los gases podían ser licuados al pagar lo que suponía trabajar a baja temperatura. Este descubrimiento animó a los investigadores a aprender las características del helio líquido. Desde que comenzaron a investigar estas características vieron que eran muy sorprendentes, sin poder explicar su comportamiento.
Para empezar, la temperatura de licuefacción de 4 2 He es la más pequeña conocida a presión normal (1 atm): -268,82°C (4,18K), es decir, cuatro grados centígrados por encima del cero absoluto. 3 Respecto al He 2, la temperatura de licuefacción es menor: -270°C (3,2K). Aunque la temperatura disminuya por completo, hasta 0,001K, por ejemplo, bajo presión ambiental no se pueden solidificar los dos isótopos del helio.
Los líquidos obtenidos a las temperaturas indicadas tienen las características de todos los líquidos, pero si la temperatura disminuye, ambos llegan al estado de superfluos. 3 El He alcanza el estado de superfluido a la temperatura 0,001K. En cuanto al 4H, alcanza su estado de superfluido a una temperatura de 2,17 K. Hoy en día, los finlandeses tienen las herramientas adecuadas para conseguir temperaturas tan bajas y mantenerlas durante mucho tiempo. En las siguientes líneas nos centraremos especialmente en las características del isótopo del helio de 4 pesos atómicos, que es el que presenta las características más peculiares.
Este isótopo del helio produce un líquido a una temperatura de 4,18K, llamado He 1. Como ya se ha comentado anteriormente, una disminución de la temperatura en torno a la temperatura de 2,17K hace que el He sufra una curiosa transformación a la que se le produce un cambio en sus características físicas. Esta transformación parece una solidificación, pero sigue siendo líquida. Si se alcanza la temperatura de 2,17 K, el 4He toma un estado de superfluido y esta nueva forma se denomina He II.
¿Cuáles son las peculiaridades de Helio II?
Por encima de la pared
La viscosidad es la propiedad de todos los fluidos, tanto de los gases como de los líquidos. La viscosidad representa la fricción interna del fluido, que transmite los efectos de un movimiento a través del fluido al unirse la dirección del mismo. La unidad es el poema (P).
La viscosidad del agua a 25°C es de 0,01 P. Los líquidos pastosos tienen una viscosidad muy elevada y los cristales son infinitos. Por el contrario, los gases presentan una viscosidad muy baja. El helio superfluido no tiene viscosidad, es decir, es completamente fluido (fluido perfecto).
Por ejemplo, una gota de aceite se desliza por un cristal más lentamente que una gota de agua. Por tanto, el aceite tiene una viscosidad mayor que el agua. Pero el helio superfluido que se conoce baja mucho más rápido que cualquier líquido normal. Una gota de helio superfluido se deslizaría por el cristal tan rápido como una bola de plomo caída en el aire desde cierta altura.
Por el contrario, a diferencia de los líquidos normales, cualquier objeto que se mueve dentro del helio superfluido no encuentra ninguna fricción.
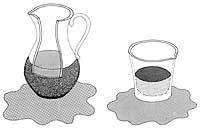
Según una ley de mecánica de fluidos, cuanto mayor es el diámetro en movimiento de un fluido, más rápido fluye. Por el contrario, He II adopta un comportamiento totalmente opuesto; en tubos de pequeño diámetro se mueve más rápido que en los grandes. Este comportamiento nos lleva a un curioso experimento: si llenáramos una jarra de cerámica sin esmaltar con helio superfluido, iría muy rápido por la pared. El agua quedaría dentro de la jarra. Por tanto, He II es un fluido tan perfecto que pasa por los poros microscópicos de la tierra quemada.
Pero, si lo guardáramos en un envase poroso, ¿qué pasaría? Podría pensarse que He II quedaría ahí, es decir, no se iría porque no hay poros. Sin embargo, esto no ocurre; comienza a subir por la pared interior del recipiente y baja por la pared exterior como si cada molécula se marchara escalando un muro. El proceso continúa hasta el vaciado del envase.

Este proceso no se llevaría a cabo por ningún líquido normal, ya que por una parte la viscosidad impide el desplazamiento capilar de las láminas del líquido y por la tensión superficial el líquido tiende a llenar el menor volumen posible y por otra parte debería superar la fuerza de gravedad sin recibir energía del exterior. Aquí se introduce el segundo principio de la termodinámica, que consiste en que el sistema autoprestado siempre pierde energía, partiendo a la situación de mayor desorden.
Así, He II supera todos los inconvenientes mencionados (viscosidad, tensión superficial, fuerza de gravedad y segundo principio de la termodinámica). El proceso se aproximaría a que una capa de pequeño espesor del superfluido comienza a elevarse por la pared interior cubriéndolo completamente. Al llegar al borde del barco comienza a descender por la pared exterior. En este momento la capa externa, bajo la influencia de la gravedad, tira de la capa interna, vaciando el recipiente. Por tanto, en el proceso He II supera las barreras de los líquidos normales antes mencionados.
No le gusta giro
Si colocamos agua o cualquier otro líquido normal en un recipiente y lo hacemos girar el recipiente, tanto vertical como horizontalmente, el agua también comenzará a girar sobre el eje de giro y con la fuerza centrífuga se formará un remolino alrededor del eje. Esto no ocurre con el helio II: Si hiciéramos girar el recipiente lleno de He II en dirección vertical o en cualquier otra dirección, el superfluido seguiría inmóvil.
Es más, no sólo con el laboratorio, sino también con las estrellas paradas, hasta que el propio laboratorio gira con la Tierra en el Espacio. El superfluido, por tanto, se encuentra completamente parado respecto a las direcciones fijas que se toman como referencia en astronomía. A pesar de que el movimiento del buque en cualquier dirección (por supuesto, se tienen en cuenta giros y traslaciones lentas y no se agitan o vuelcan el barco), el He cumple esta característica. En este experimento He II es una referencia estable respecto a todos los movimientos del envase y se comporta como una peonza giroscópica.
Dado que el helio superfluido no tiene viscosidad, no tiene adherencia ni fuerza resistente al desplazamiento con las paredes del buque, es decir, al no afectar al helio superfluido, cumple el principio de inercia. En primer lugar, veamos lo que dice este principio: un punto material que no está influenciado por ninguna fuerza está parado o se mueve con un movimiento rectilíneo uniforme. Como consecuencia de este príncipe tenemos la propiedad de la materia llamada inercia. Esta propiedad indica que un cuerpo no puede cambiar de forma natural su estado de movimiento o reposo. Dado que al helio superfluido no se le transmite ninguna fuerza externa por fricción, He II sigue inmóvil según el principio de inercia, una vez que el envase ha comenzado a moverse.
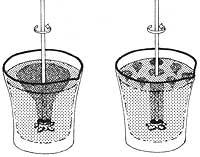
Por otra parte, si se desplazara el helio superfluido, según el principio de inercia, éste debería moverse con un movimiento rectilíneo uniforme, ya que, como se ha indicado anteriormente, no existe fuerza resistente al desplazamiento. Esta afirmación puede demostrarse con el siguiente experimento: desde que el He II se desplome en el interior de un tubo largo y cerrado, el He II se moverá continuamente en el tubo realizando una corriente interna permanente, al igual que las corrientes eléctricas permanentes se desplazan en superconductores.
Comportamiento frente al calor
Cuando el calor se propaga fácilmente por el interior de un cuerpo, se dice que es un buen conductor de calor. Por el contrario, es un mal conductor de calor cuando es difícil de expandir. Por tanto, cuando un cuerpo conduce fácilmente el calor presenta una elevada conductividad térmica. La conductividad térmica es la propiedad que nos indica cómo un cuerpo lleva el calor.
En los fluidos, cada molécula puede desplazarse de un punto a otro, es decir, se mueve. Mediante este movimiento se propaga el calor a través del fluido.
Cuando un líquido normal se somete a una fuente de calor, cuanto más cerca esté cualquier punto del líquido de la fuente de calor, más caliente es, es decir, el líquido se calienta localmente. Por tanto, dentro del líquido se generan diferencias. El calor se extiende desde los puntos calientes hasta los más fríos, y cuanto mayor sea la diferencia entre los puntos, más rápido y más rápido.
El superfluido helio no se comporta como se ha dicho antes ante el calor. Por un lado, su conductividad térmica es infinita, y ésta es cada vez mayor, cuanto menor sea la diferencia entre puntos. Por otro lado, al no producirse un punto caliente en el fondo del helio superfluido, éste no hierve. Sin embargo, al calentarse se aromatiza, pero la evaporación se produce en la superficie, quedando el resto del fluido a la misma temperatura. En la práctica, por lo tanto, aparece como un superconductor de calor, es decir, si se producen pequeñas diferencias, el calor se propaga rápidamente a través del líquido. Por ello, el calentamiento o enfriamiento local es prácticamente imposible. Por lo tanto, dentro del líquido no se pueden producir desigualdades.
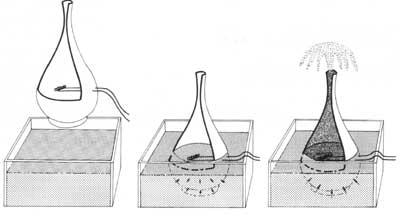
Para conocer la propagación del calor a través del helio superfluido se ideó el siguiente experimento: si en un baño de helio superfluido se introduce un recipiente con poros y cuello apretado, el helio superfluido penetra por los poros, dando por finalizado el proceso de penetración cuando se encuentran a la misma altura exterior e interior. Si posteriormente calentáramos el interior del recipiente con una resistencia eléctrica, el superfluido que lo rodea entraría a través de la pared para enfriar el interior y mantener el equilibrio. Debido a la cantidad de helio que entra en el envase, la gran chorreada de helio sale del cuello del envase para eliminar la diferencia de masa.
Los investigadores han reconstruido este experimento creando calores cortos a base de una resistencia eléctrica. Estos calentamientos provocan que el calor se expanda como ondas a través de la masa líquida. Estas ondas se denominan ecos secundarios. Esta forma de propagación del calor no se cumple en ninguna otra condición.
Como conclusión
Entre otras cosas, todos los experimentos realizados con 4 He podrían realizarse con 3 He, pero habría que trabajar a temperaturas más frías, 0,001K alrededor de la temperatura. 3 El He presenta propiedades muy sorprendentes: puede ser solidificado bajo determinadas presiones, pero no enfriándose, sino calentándose. Además, el superfluido 3 He es magnético, al igual que el hierro o el níquel, y los experimentos realizados demuestran dos tipos: 3A y 3B. 3A La densidad del helio (con mayor imantación) es muy difícil de calcular debido a su variabilidad. La densidad varía en función del campo magnético que atraviesa el superfluido.
Para terminar, la situación superfluida interesa profundamente a los astrónomos, ya que explica el comportamiento de las estrellas de neutrón. En ellas hay una capa de neutrones que no es sólida, líquida ni gaseosa, sino superfluo. Por tanto, los estudios que se están llevando a cabo en los laboratorios crioscópicos nos llevan a un cielo que no se ve afectado por la materia.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian











