Maladies cardiovasculaires: physiopathologie et nouveaux traitements
Les maladies cardiovasculaires sont un ensemble de troubles cardiovasculaires qui ont comme cause principale une pathologie appelée athérosclérose qui se développe par accumulation de cholestérol dans les artères. Cette revue décrit la physiopathologie de l'athérosclérose et les nouveaux traitements proposés.
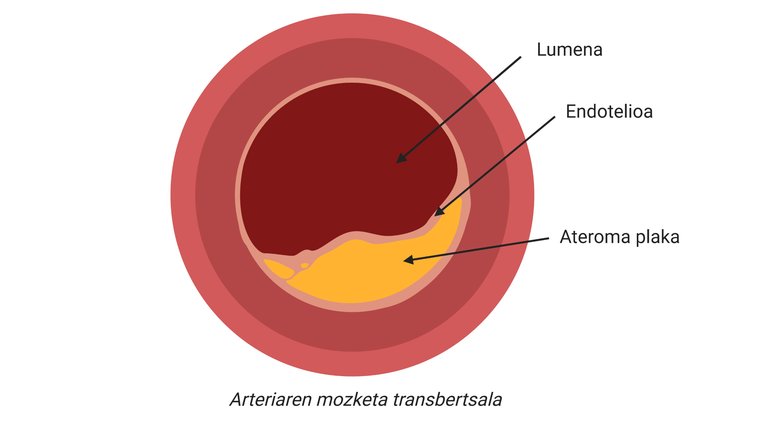
Les maladies cardiovasculaires (GKB) sont l'ensemble des maladies qui engendrent le plus de décès. Chaque année, 17,9 millions de personnes meurent, principalement par infarctus et infarts1. De plus, contrairement à ce que l'on croit habituellement, l'incidence de GKB n'est pas seulement une caractéristique propre aux pays à revenu élevé.
Les facteurs de risque comprennent des facteurs génétiques ou dépendants de l'âge tels que l'hypertension, le cholestérol élevé et le glucose dans le sang et le surpoids. D'autre part, les habitudes comportementales qui sont entre nos mains : un régime aliéné, une consommation nocive de tabac et d'alcool et des activités physiques inadéquates. En fait, la plupart des infarctus et du cœur peuvent être évités en améliorant les habitudes de vie et, bien sûr, en recevant un traitement approprié si nécessaire.
Enfin, la situation économique personnelle et le degré de développement du pays de résidence ont beaucoup à voir tant dans la détection que dans le traitement des maladies. Ainsi, plus de trois patients atteints de GKB sur quatre sont actuellement diagnostiqués dans les pays sous-développés, selon l'Organisation mondiale de la santé 1.
Comment se produisent les infarctus?
Les infarctus et les infarctus sont des complications cliniques de l'athérosclérose, une des principales causes de maladies cardiovasculaires, caractérisée par l'accumulation de cholestérol et des éléments fibreux dans les artères principales.
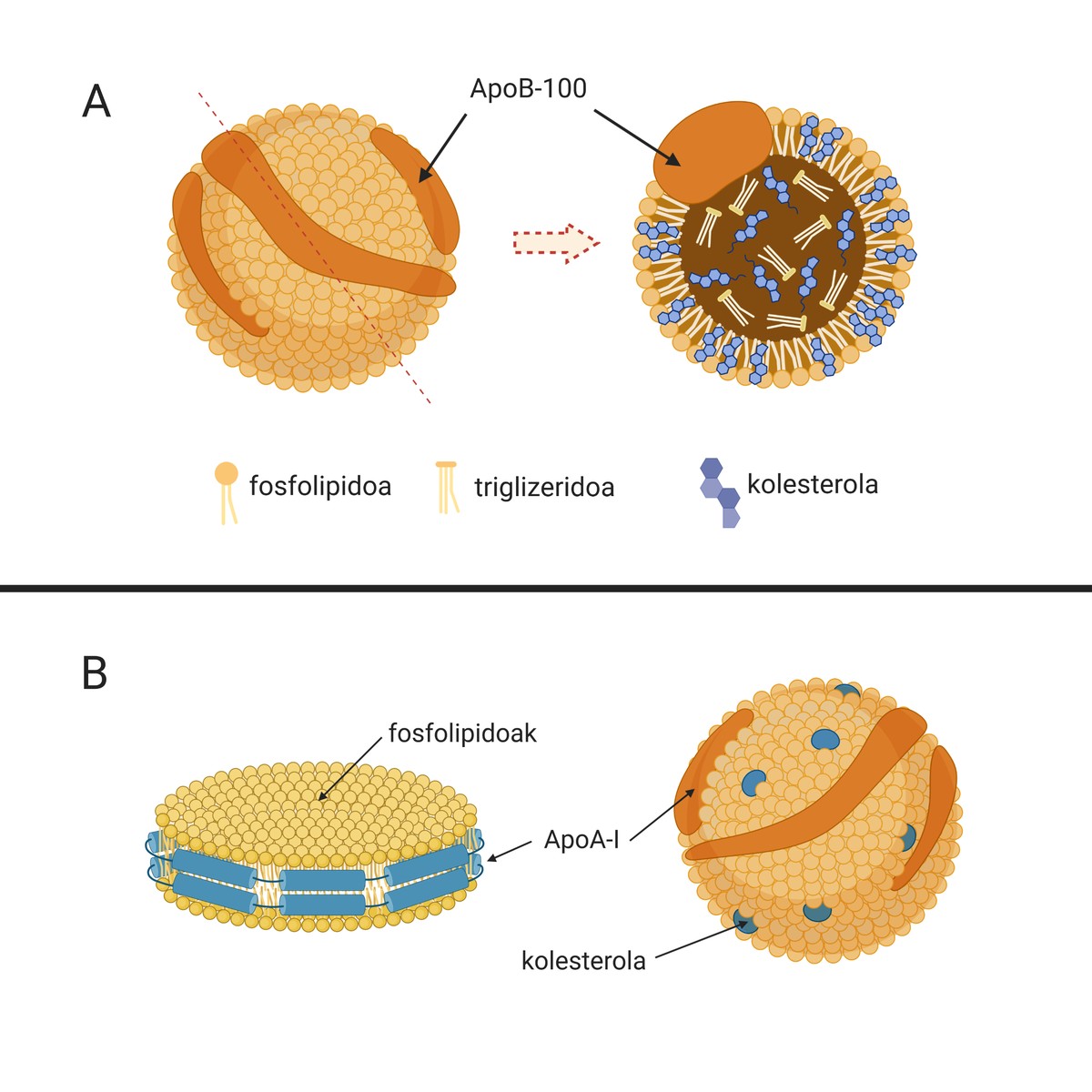
Les causes de cette maladie sont les lipoprotéines à faible densité ou les particules naturelles appelées LDL (de l'anglais Low Density Lipoprotein), appelées «mauvais cholestérol». Ces particules (A.1. L'image est composée de lipides et d'apolipoprotéines qui sont chargés du transport du cholestérol du foie (organe chargé de la synthèse de la majeure partie du cholestérol endogène) à d'autres tissus pour leur alimentation. En fait, le cholestérol est une molécule indispensable pour de nombreux processus cellulaires. Mais si c'est le cas, pourquoi avez-vous le surnom de “mauvais cholestérol”?
Les particules LDL sont capables de traverser l'endothélium des artères corporelles et de le stocker sous lui, ce qui peut être préjudiciable, surtout chez les personnes ayant un degré élevé de LDL dans le sang (par exemple chez les patients souffrant d'hypercholestérolémie).
En fait, une fois que les LDL sont dans l'artère, ils commencent à s'oxyder en devenant LDL oxydé (LDL ox), car il n'y a pas d'antioxydants présents dans le sang (Figure 2). Par conséquent, les macrophages, les cellules responsables du nettoyage de notre corps, intérioriseront les particules LDL au moyen de récepteurs, car elles détectent qu'elles sont nocives pour l'organisme, c'est-à-dire qu'elles seront chargées de leur élimination. Si l'accumulation de LDL est trop élevée, les macrophages continueront à s'intérioriser par des mécanismes non réglementaires et les gouttes de cholestérol s'accumuleront à l'intérieur. Face à une situation incontrôlable, ils attireront d'autres types de cellules et mettront en place des mécanismes inflammatoires dans lesquels on commencera à développer l'athérosclérose (Figure 2).
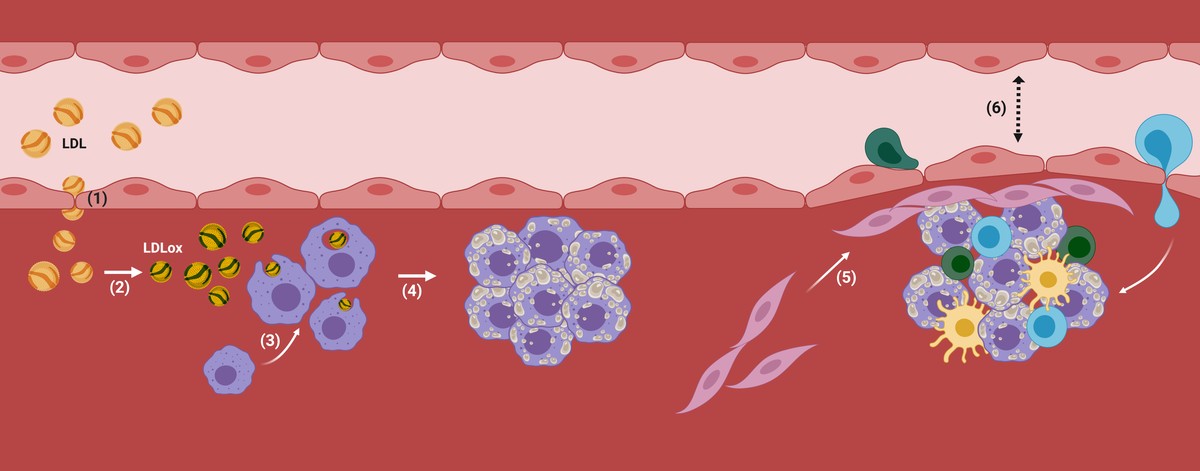
Ainsi, plus de cholestérol et certains types de cellules seront accumulés dans la zone subdoteliale de l'artère. En outre, il commencera à couvrir la plaque avec un matériau rigide produite par les cellules pour empêcher la lésion produite de se verser dans le flux sanguin. Avec le passage du temps, cette zone de l'artère sera de plus en plus large et donc le diamètre du vaisseau sanguin sera plus étroit. Voici la plaque athérosclérotique (Figure 2).
Il faut dire que dans des situations physiologiques on peut éviter le développement de cette plaque, puisque notre organisme dispose de mécanismes pour éviter son développement. Il s'agit notamment de lipoprotéines à haute densité ou de particules lipidiques appelées HDL (de l'anglais High Density Lipoprotein) (1.B. ). Image). Ce sont aussi des particules naturelles qui se chargent du transport du cholestérol, mais dans ce cas, elles mènent un processus contre les LDL: elles recueillent le cholestérol excédentaire des tissus périphériques et le transportent au foie pour leur excrétion. Ce processus est appelé transport inverse du cholestérol. Cependant, nous approfondirons plus tard l'importance des HDL dans l'athérosclérose.
La vraie complication clinique peut se produire quand une partie de la plaque d'athérome est déstabilisée et libérée, car un trombe ou un caillot est formé. C'est parce que le thrombus peut bloquer un vaisseau sanguin, de sorte que le tissu entourant le vaisseau va commencer à mourir par manque d'oxygène. Ainsi, nous appelons infarctus à la mort de ce tissu et, si elle se produit dans le cœur, à l'infarctus.
Il n'y a pas encore de médicaments qui traitent directement l'athérosclérose, qui implique la réduction de la plaque d'athérome. Par conséquent, le traitement de la maladie est basée sur la réduction des niveaux de LDL dans le sang, en utilisant pour cela des statines connues, afin de prévenir plus que le traitement de l'athérosclérose.
D'autre part, les personnes diagnostiquées d'athérosclérose sont suivies de la plaque et quand ils peuvent supposer un risque pour le patient sont généralement enlevés avec des méthodes invasives. Une de ces méthodes invasives est l'endarterectomie, qui consiste à enlever la plaque d'athérome par une intervention chirurgicale.
Mais est-il possible d'enlever la plaque d'athérome?
Depuis plusieurs années, on étudie les médicaments qui visent à freiner le développement de l'athérosclérose et à éliminer la plaque d'athérome, jusqu'à ceux qui ont été conduits à des essais cliniques aussi divers que les processus impliqués dans le développement de l'athérosclérosion3. Cependant, son degré de succès prouve qu'il n'a pas encore trouvé la clé pour traiter l'athérosclérose.
Plusieurs médicaments ont été proposés, entre autres, pour éviter l'oxydation des LDL, mais, bien qu'ils fonctionnent en laboratoire, aucun résultat significatif n'a été obtenu chez les patients. Les vitamines antioxydantes (vitamines C, D et E) ont également été testées dans de grands essais cliniques, sans meilleurs résultats.
D'autre part, des essais ont été menés pour réduire l'inflammation. Par exemple, l'essai clinique CANTOS, achevé en 2017, a démontré son efficacité chez les patients atteints du syndrome coronaire aigu. Cet essai a utilisé un anticorps appelé canakinumab, qui réduit l'inflammation et avec lui les épisodes cardiovasculaires. Cependant, l'incidence des infections mortelles a été plus élevée dans le groupe traité avec canaquinumab par rapport au groupe de placebos, et il a fallu exclure le traitement.
Récemment, l'immunothérapie a également été proposée, comme l'utilisation de molécules naturelles qui stimulent la protection du système immunitaire. Par exemple, dans l'essai clinique LILAC actuellement en cours, l'administration de faibles doses d'interleucine IL-2 a été proposée afin d'induire la stabilité de la plaque d'athérome.
HDL comme nouveau traitement de l'athérosclérose
Comme mentionné précédemment, pour faire face au développement de la plaque d'athérome, il existe des particules naturelles appelées HDL, responsables du transport inverse du cholestérol. En fait, les HDL recueillent du tissu corporel (et aussi de la plaque) le cholestérol restant et le transportent au foie pour qu'il soit éliminé avec la bile. Par conséquent, les HDL sont appelés “bon cholestérol”.
Comme les LDL, les HDL sont capables de traverser la paroi artérielle (car ils sont beaucoup plus petits en taille) et de remplir leur fonction (3.A. Image), recueillent le cholestérol des macrophages qui commencent à s'accumuler dans l'artère. Pour ce faire, l'apolipoprotéine apoA-I présente dans les HDL interagit avec les récepteurs de la membrane cellulaire des macrophages, qui, fonctionnant comme canal, passeront au HDL un cholestérol restant (3.B. Image). Ensuite, pleines de cholestérol, les particules HDL retourneront dans le sang vers le foie.
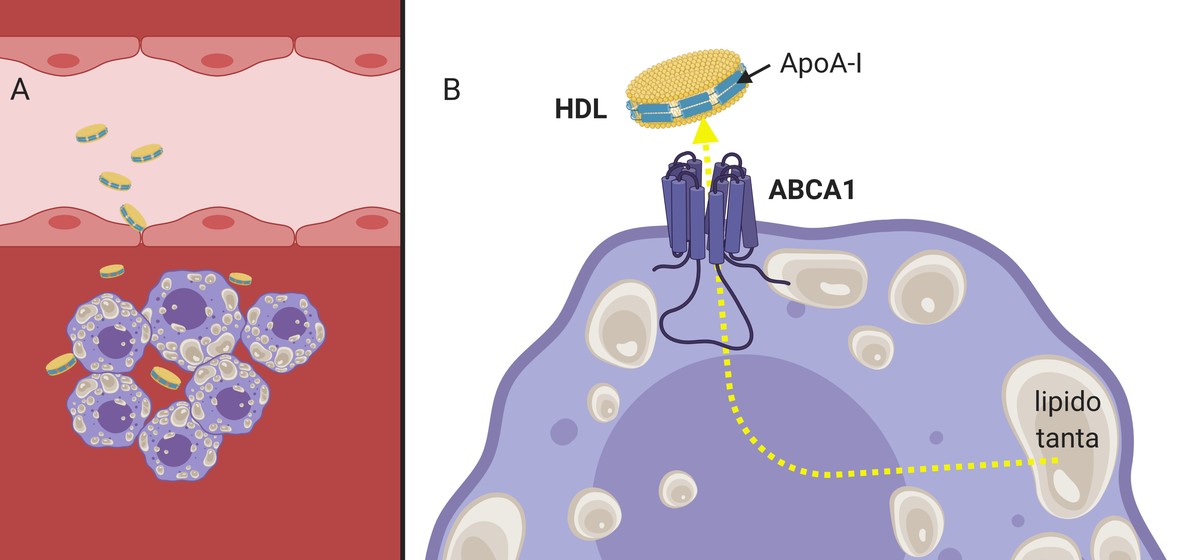
Il a été démontré que, en plus d'induire l'efflux ou le flux vers l'extérieur du cholestérol, les HDL sont en mesure de réduire les signaux inflammatoires sur la plaque ateroma3. Pour toutes ces caractéristiques, les particules HDL sont considérées comme protectrices de sac. Il n'est donc pas étrange que de nombreux groupes de recherche aient synthétisé dans le laboratoire HDL afin d'induire l'élimination du cholestérol.
Les premières particules in vitro HDL ont été formées dans les années 70 et 80; les rHDL à partir de maintenant (reconsituted HDL). Pour sa synthèse, la principale protéine de HDL, apoA-I et plusieurs mélanges lipides4 ont été utilisés. De cette façon, des particules discoïdales à nanoéchelle ont été obtenues qui ont le même aspect que les HDL naturels. Depuis lors, de nombreuses combinaisons de RHDL ont été publiées et sa fonctionnalité a été mesurée en prenant le cholestérol des cellules de la plaque d'athérome. Ils ont eu un excellent succès 5,6.
Des études in vitro, on est passé aux études in vivo par des essais cliniques, les premiers rHDL testés chez les humains, les essais cliniques appelés MILANO-PILOT, qui ont pris fin en 2016. Au cours de cet essai, une fois par semaine, une certaine quantité de ces nanoparticules a été fournie aux patients par injection intraveineuse. Cependant, ils n'ont pas obtenu des résultats significatifs en réduisant la plaque d'athérome et ont dû suspendre l'essai clinique.
Par la suite, d'autres essais ont été menés, et un essai clinique en cours teste actuellement une nouvelle composition lipidique de rHDL, qui devrait accroître l'efficacité. Pour connaître vos résultats, vous devez attendre l'année prochaine.
Il convient de noter que des essais intéressants sont en cours pour l'utilisation de particules rHDL dans le traitement du cancer. Dans ces cas, cependant, les rHDL sont utilisés comme système de transport de médicaments contre le cancer, car le composé actif est inclus dans la nanoparticule. Cette formulation devrait minimiser les effets secondaires graves en chimiothérapie, car ils ont montré que les RHDL ont une spécificité tumorale. Autrement dit, le transport du médicament dans la nanoparticule réduirait la libération de plasma et réduirait donc les effets indésirables sur d'autres tissus. En outre, s'il s'agit d'un traitement corrigé, des doses inférieures à la normale peuvent être utilisées, obtenant le même effet contre le cancer.
Cependant, dans les maladies cardiovasculaires, l'utilisation de rHDL n'a pas encore été étendue à des essais cliniques. Il existe des études in vitro sur les formulations rHDL qui transportent des statines, mais aucune preuve clinique n'a été proposée pour l'instant. Et vu que jusqu'à présent les essais visant à induire l'efflux de cholestérol n'ont pas obtenu des résultats escomptées12–14, il serait intéressant de réaliser cette proposition.
BIBLIOGRAPHIE
1.World Health Organization. https://www.who.int/health-topics/cardiovasculaire diseases
2.Linton, M. F. et al. The Role of Lipids and Lipoproteins in Atherosclerosis. Endotext (eds. Feingold, K. R. et al.) (MDT ext.com, Inc., 2000), South Dartmouth (MA).
3.Navab, M., Reddy, S. T., Van Lenten, B. J. et Fogelman, A. M. 2011. HDL and cardiovasculaire disease: atherogenic and atheroprotective mechanisms. Nat. Rev. Cardiol. 8, 222–232.
4ºMatz, C. E. et Jonas, A. 1982. "Complexes Micellar of human apolipoprotein A-I with phosphatidylcholines and cholesterprepared from cholate-lipid dispersions". J. Biol. Chem. 257, 4535–4540.
5.Tang, J. et al. 2016 "Immunisé cell screening of a nanoparticle library improves atherosclerosis therapy". Proc. Natl. Acad. Sci. 113, E6731–E6740.
6ºCukier, A. M. O. et al. 2017 "Structure-function relationships in reconstituted HDL: Focus on antioxyative activity and cholesterefflux capacity". Biochim. Biophys. Acta Mol Cell Biol. Lipids 1862, 890–900.
7.Gibson, C. M. et al. 2019. "The CSL112-2001 trial: Safety and tolability of multiple doses of CSL112 (apolipoprotein A-I [human]), an intravenous formulation of plasma-dérived apolipoprotein A-I, among subjects with moderate renal aimants after acute myocardial infarction". Am. J. Heart 208, 81–90.
8º. Sabnis, N., Pratap, S., Akopova, I., Bowman, P. W. et Lacko, A. G. 2013 Pré-Clinical Evaluation of rHDL Encapsulated Retinoids for the Treatment of Neuroblastoma. Front. Pédiatrie. 1°, 6°
9.Morin, E. R. Li, X. et Schwdémonan, A. 2018. "HDL in Endocrine Carcinomes: Biomarqueur, Drug Carrier, and Potential Therapeutic». Front. Endocrinol. 9, 715.
10. Raut, S. et al. 2018. "Reconstituted HDL: Drug Delivery Platform for Overcoming Biological Barriers to Cancer Therapy". Front. Pharmacol. 9, 1154.
11.Duivenvoorden, R. et al. 2014 "A statin-loaded reconstituted high-density lipoprotein nanoparticle inhibits atherosclerotic inflammation". Nat. Commune. 5, 3065.
12. Nicholls, S. J. et al. 2018. "Effect of Infusion of High-Density Lipoprotein Mimetic Containing Recombinant Apolipoprotein A-I Milano on Coronary Disease in Patients With an Acute Coronary Syndrome in the MILANO-PILOT Trial: A Randomized Clinical Trial». JAMA Cardiol. 3, 806-814.
13. Nicholls, S. J. et al. 2018. "Effect of Serial Infusions of CER-001, a Pre-b High-Density Lipoprotein Mimetic, on Coronary Atherosclerosis in Patients Following Acute Coronary Syndromes in the CER-001 Atherosclerosis Neacute Regrsion Tracense: A Randomized Clinical Trial». JAMA Cardiol. 3, 815.
14.Tardif, J.-C. et al. 2007 "Effects of Reconstituted High-Density Lipoprotein Infusions on Coronary Atherosclerosis". JAMA Cardiol. 297, 1675.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian











