Zorionak a tu, zorionak Henrietta?
L'any 2020, tan especial i exigent per a tots, en el qual el covid-19 ha liderat gairebé totes les notícies, ha quedat fora dels focus (sota el nostre criteri) un aniversari, el 100 aniversari del naixement d'Henrietta Lacks. Encara que la vida d'Henrietta va ser curta i senzilla, les seves cèl·lules no sols ajuden a dominar el covid-19, sinó que ajuden a comprendre i analitzar les causes d'altres malalties. Aquestes cèl·lules s'han convertit en un instrument de vital importància. Aquest és el nostre petit homenatge.

L'any 2020 es compleixen 100 anys del naixement del bertsolari Xalbador, del saxofonista Charlie Parker i del cineasta Ray Harryhaus, entre altres. Al costat d'aquests famosos personatges, s'ha complert també el centenari del naixement d'Henrietta Lacks, menys conegut. Malgrat la seva menor fama, Henrietta ha tingut una gran importància en nombrosos estudis biomèdics. Gràcies a ella, es va crear una vacuna contra la poliomielitis i s'han realitzat diversos descobriments per a combatre la sida, la malaltia de Parkinson, el papilomabirus humà, el càncer, etc. De fet, almenys mitja dotzena de premis Nobel li deuen en part el seu reconeixement.
Però, com ha arribat a ser un pilar fonamental en la recerca d'alt nivell aquest tabaquer que va morir als 31 anys?Henrietta, en 1951, es va acostar a l'hospital John Hopkins de Baltimore i a l'entrada de la clínica ginecològica va dir “I got a> k in my womb” (tinc un nus en l'utero). Després de l'exploració inicial, van trobar una massa densa en el coll uterí d'Henrietta, de la qual, com era habitual en l'època, van obtenir una mostra i la van portar al laboratori de patologia de l'hospital per a realitzar un diagnòstic més profund. En aquella època, el laboratori estava dirigit pel matrimoni George-Otto Gey i Margaret Koudelka.
George, investigador del càncer, necessitava constantment noves cèl·lules per als seus assajos, ja que en condicions in vitro la majoria de les cèl·lules murían relativament ràpid (encara que Margaret era un expert en el manteniment de les cèl·lules i en el manteniment de les condicions d'asèpsia dels laboratoris). Però les cèl·lules obtingudes del tumor d'Henrietta, no obstant això, es dividien cada 24 hores i no deixaven de fragmentar-se. George va quedar fascinat i, com era habitual, va nomenar a aquestes cèl·lules recentment obtingudes combinant el nom i cognoms del pacient com a cèl·lules HeLa. Mentrestant, Henrietta va morir 10 mesos després de la seva primera visita a l'hospital, mentre les seves cèl·lules canceroses continuaven fragmentant-se en els laboratoris.
Quan va descobrir que tenia entre les seves mans una eina amb un gran potencial, George va començar a distribuir cèl·lules de forma àmplia i lliure als laboratoris dels Estats Units. És de destacar que George també va lliurar mostres de cèl·lules HeLa a diversos laboratoris abans de realitzar recerques amb cèl·lules HeLa. George Gey era més investigador o empresari que professor i va tractar les cèl·lules d'Henrietta com a regal científic.
A pesar que el viatge més llarg que va realitzar Henrietta durant la seva vida va ser el mitjà entre Clover (Virgínia) i Baltimore (Maryland), uns 400 quilòmetres, les seves cèl·lules han arribat a tots els racons del món, han viatjat milers de quilòmetres per laboratori. Arriben a l'espai! Tant en MIR com en l'Estació Espacial Internacional.
Al marge dels quilòmetres, els diners també té molt a dir en aquesta història. En la pàgina web de l'ATCC (American Type Culture Collection), per exemple, quan se sol·liciten cèl·lules com “HeLa (ATCC® CCL-2TM)”, el tub cel·lular té un cost de 595€ + transport. Les cèl·lules d'Henrietta, des de 1954, han generat milions i milions d'euros per a les empreses farmacèutiques, la qual cosa ha permès avanços mèdics espectaculars. No obstant això, ni Henrietta ni els seus 5 fills van tenir assegurança mèdica. Com s'ha esmentat anteriorment, Henrietta va signar l'imprès de tractament convencional, però no se li va donar el consentiment escrit per a l'obtenció de mostres de biòpsia i mai se li va explicar què es va fer amb les seves cèl·lules cancerígenes. Es va seguir el procediment de l'any 1951 i el fet de ser dona i negre de pell no el va ajudar a garantir els seus drets.
Aquestes cèl·lules, a més d'estar disperses per tots els laboratoris del món, són capaços de contaminar altres cultius cel·lulars. En els anys 1960-70, i suposant que diversos investigadors estaven treballant amb altres tipus de cèl·lules, es van adonar que en els seus envasos de cria tenien cèl·lules HeLa! Les cèl·lules d'Henrietta tenien una gran capacitat de fragmentació, la qual cosa permetia la substitució de les cèl·lules originals de l'envàs. Això va despertar l'interès dels investigadors per les cèl·lules d'HeLa, que van començar a preguntar-se pel seu origen. Qui era, per tant, el malalt que estava darrere del nom de “HeLa”? Al principi, el laboratori del matrimoni Gey, amb l'objectiu d'ocultar el seu nom original, li van donar altres pseudònims (Helen Lane o Helen Larsen) a investigadors i periodistes que buscaven el seu origen. No obstant això, el secret no va poder mantenir-se. No obstant això, els familiars d'Henrietta van haver d'esperar encara més per a conèixer-ho i més per a comprendre la importància del descobriment.
En l'actualitat, quan els teixits d'un pacient s'adquireixen per a la recerca, és necessari que el malalt doni el seu consentiment escrit. Una vegada obtinguda la mostra passa a ser anònima i el donant, el pacient, no és propietari de la mostra. És a dir, el malalt no té drets futurs sobre els ingressos que puguin derivar-se d'aquests teixits.
Aquesta situació, no obstant això, va canviar notablement en 2013. G3: En la revista Gens, Genomes, Genetics es va publicar la caracterització genòmica d'un cep de cèl·lules HeLa (Landry et al., 2013) i es va posar a disposició tot el genoma online. Això és molt interessant per als investigadors, però té moltes incidències ètiques. A pesar que les cèl·lules d'HeLa han mutat molt després de 62 anys, la informació genètica d'Henrietta i els seus familiars va quedar públicament disponible. Després d'eliminar la seqüencia genòmica d'una coneguda base de dades, el Laboratori Europeu de Biologia Molecular (EMBL), l'Institut Nacional de Salut dels Estats Units (NIH) i la família Lacks van arribar a un acord sobre l'ús de cèl·lules HeLa.
Desgraciadament, la família Lacks no és l'únic cas, en l'actualitat existeixen milers de línies cel·lulars i els avanços en seqüenciació i bioinformática permeten qüestionar l'anonimat dels donants. Per tant, és cada vegada més necessari fomentar les relacions entre donants, investigadors i institucions.
Transformació cel·lular de l'henrietta
Les cèl·lules tumorals de l'henrietta tenen el seu origen en un papilomavirus humà (HPV). La cèl·lula interioritza aquests virus mitjançant processos cel·lulars d'endocitosis i posteriorment l'ADN víric s'integra en l'ADN de la cèl·lula hoste. En el cas de l'henrietta, aquesta injecció d'ADN víric va tenir lloc prop del gen c-myc. Sent C-myc un dels gens més importants que impulsa la divisió cel·lular, permet expressar HeLa de manera constant (contínua) en les cèl·lules, per la qual cosa la divisió cel·lular s'impulsa constantment. D'altra banda, HeLa és l'alta activitat de la telomerosis en les cèl·lules. Els telómeros són els extrems dels cromosomes estabilitzats per telomasas. Quan es produeixen divisions de cèl·lules, els telómeros es van escurçant i, quan s'aconsegueix una grandària crítica, deixen de dividir les cèl·lules o tenen més dificultats per a dividir-les. Per a l'estirament dels telómeros és necessària l'activitat de l'enzim telomerasa, per la qual cosa en el cas de les cèl·lules d'HeLa, malgrat haver realitzat nombroses divisions, els telómeros són prou llargs per a poder continuar produint la divisió cel·lular.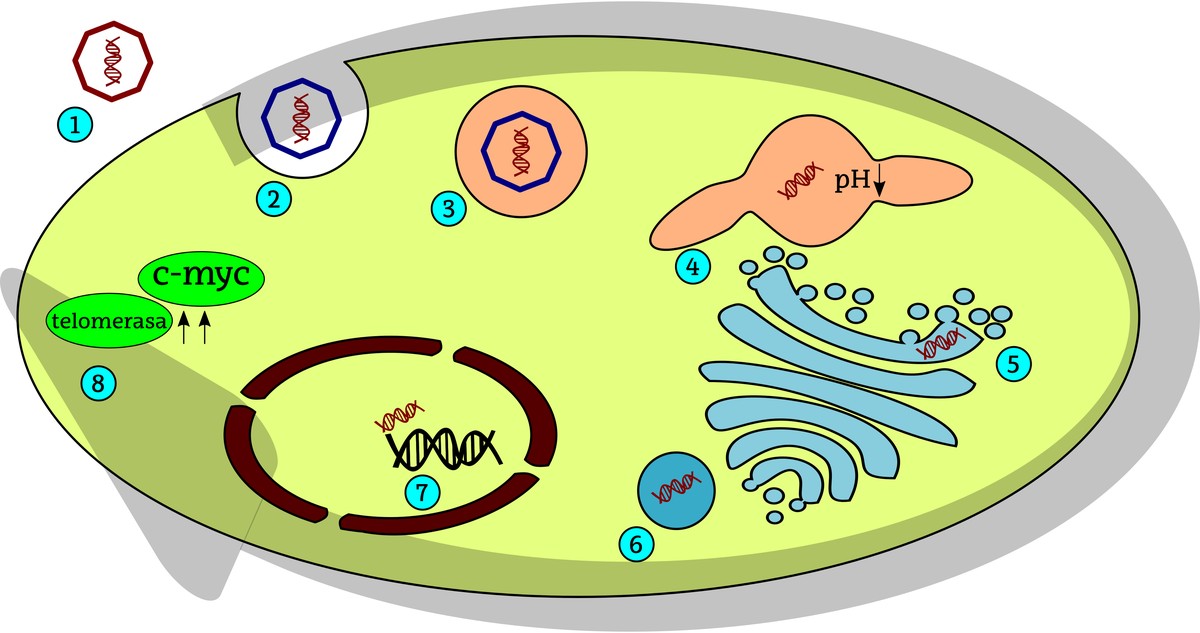
Henrietta va néixer fa 100 anys i va morir fa 69 mesos, però les seves cèl·lules continuen vives en laboratoris de tot el món. Les cèl·lules d'HeLa no responen a les preguntes personals que Deborah, la filla d'Henrietta, té sobre la seva mare (quin era el color favorit de la seva mare? Li agradava ballar? ), però ajudaran a resoldre altres qüestions científiques. Un sap si les seves cèl·lules continuaran celebrant per sempre.
Gràcies per la seva aportació a la ciència i enhorabona a Henrietta!
Lectura addicional:
Landry JJ, Pyl PT, Rausch T, Zichner T, Tekkedil MM, Stütz AM, Jauch A, Aiyar RS, Pau G, Delhomme N, Gagneur J, Korbel JO, Huber Lw. 2013 "The genomic and transcriptomic landscape of a HeLa cell line". G3: Gens, Genomes, Genetics. 3 (8): 24-1213.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian