Inmunología de los trasplantes
A esta conclusión se llega gracias a una serie de datos.
Por un lado, el rechazo al trasplante no es quirúrgico, ya que las mejoras en las técnicas quirúrgicas no han coincidido con el porcentaje de éxito (todavía es relativamente bajo).
Por otra parte, el rechazo es inmunológico porque cumple las características de la Inmunidad Adaptativa: memoria y especificidad.
¿Qué son estos?
Se entiende por memoria inmunológica, aquella en la que el receptor rechaza más rápido y vigorosamente la segunda vacuna tomada del mismo donante que la primera (Figura 1).
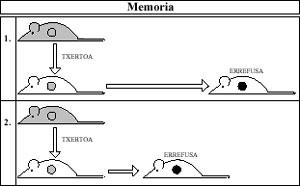
El Sistema Inmune recuerda el primer contacto con la vacuna y en el segundo los mecanismos están dispuestos a actuar de forma más violenta contra el rechazo.
La especificidad es que el segundo rechazo es más rápido y vivo contra las vacunas que se reciben del mismo donante, pero no contra las que se reciben de cualquier otro donante (Figura 2).
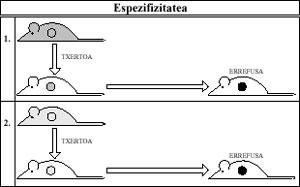
Cuando el Sistema Inmune entra en contacto con una vacuna (antígeno), sólo se sensibiliza contra esta vacuna específica.
Existen otros datos que atribuyen al Sistema Inmune la capacidad de rechazar. Por ejemplo, al no llegar las células inmunes a algunos órganos y/o tejidos del cuerpo (ojo, hueso, cartílago), estos tejidos pueden insertarse sin ningún tipo de problema, ya que el rechazo es raro.
Base inmunológica del rechazo
En general, el rechazo de la vacuna consiste en que el Sistema Inmune del receptor es capaz de ver de forma extraña a las células de la vacuna y a continuación proceder al ataque. Después el tejido insertado muere, es decir, es rechazado.
Antígenos de Histocompatibilidad (HLA Ag)
El receptor es capaz de ver de forma extraña las células de la vacuna a través de diversas moléculas que las contienen en su superficie. Estas moléculas se denominan Antígenos de Histocompatibilidad.
Son antígenos porque son capaces de producir una respuesta inmune como cualquier otro antígeno. También son de histoconjugación, ya que intervienen en los fenómenos de aceptación de la vacuna (conjugación) o rechazo (inconjugación).
Estos compuestos son de dos tipos (clase I y clase II) y distintos, tanto en su morfología como en su función.
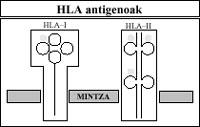
Bioquímicamente tenemos glicoproteínas ancladas a la membrana celular. Las moléculas de la clase I están formadas por dos cadenas pepídicas de diferente peso. Por el contrario, las moléculas de la clase II están formadas por dos cadenas pepitorias de peso similar. Estos contienen tres hidratos de carbono.
A pesar de desempeñar un papel muy importante en el rechazo al trasplante, la función original de los antígenos HLA no es, lógicamente, esta, ya que en la Naturaleza no se produce un trasplante. Su función real es ser diana para el Sistema Inmune.
Gracias a ellos, las células inmunes del individuo son capaces de distinguir entre su propia y su extraña. Es decir, las propias células inmunes consideran propias a las demás células del cuerpo porque consideran propias a los antígenos HLA que contienen en la membrana.
Y, de media, ven extrañas las células de la vacuna porque ven extraños sus antígenos HLA.
Por tanto, los antígenos HLA actúan como documento de identidad.
Estos antígenos intervienen en funciones de gran importancia como (1) las interacciones entre células del Sistema Inmune, (2) la eliminación de células extrañas y (3) la destrucción de células propias pavimentadas o alteradas.
1.
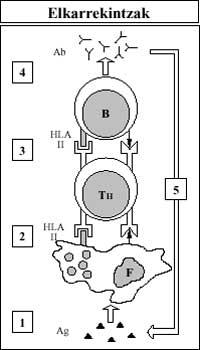
Cuando una sustancia extraña (Ag) entra en el cuerpo, las células del Sistema Inmune son conocidas por los antígenos HLA-II, dando una respuesta coordinada a esta sustancia. El fagocito (F) asume el antígeno extraño y lo presenta junto con su antígeno cutáneo HLA-II al Ayudante Linfocito T (T H). El ayudante T induce entonces al linfocito B (B) conociendo los mismos antígenos presentes en la membrana de esta última célula (extraño y HLA-II). Por último, el linfocito B produce anticuerpos (Ab) que agarran al antígeno extraño y lo eliminan. (Figura 4).
2.
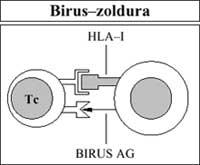
Asimismo, las células inmunes (concretamente los linfocitos T citotóxicos), con la ayuda de los antígenos HLA-I, ven lorrin a las células propias pavimentadas (infección viral) o alteradas (cáncer). A continuación se procede a su eliminación (Figura 5).
3.
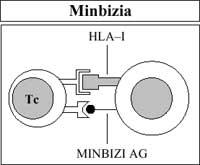
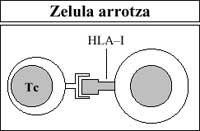
Asimismo, los linfocitos T citotóxicos destruyen (rechazan) la vacuna o el trasplante extraño tras ser considerados como extraños por el antígeno HLA-I de su membrana (Figura 6).
Mientras que las dos primeras funciones son naturales, es decir, desde que se creó el hombre se sientan, este tercero es totalmente artificial, ya que los trasplantes sólo se han realizado en el último siglo. Más adelante aparece este último punto, que es una de las claves del artículo.
Histocompatibilidad Compleja Principal (MHC)
Como todas las proteínas, los antígenos HLA son codificados por un haz de genes (genes HLA). Estos genes se encuentran en una pequeña parte del cromosoma 6 del ser humano, en la denominada Histocompatibilidad Compleja Principal.
Esta zona está formada por cinco subáreas. Tres de ellos codifican los antígenos -A, B y Ck-HLA-I. El cuarto codifica los antígenos -D-HLA-II. Por su parte, el subfoco intermedio codifica algunos factores solubles distintos de los antígenos HLA pero relacionados con la respuesta inmune (Figura 7).
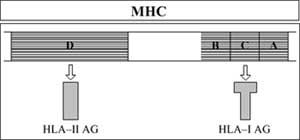
Los genes HLA son muy polimórficos, es decir, cada uno tiene alelos diferentes. La combinación de todos estos alelos da lugar a un gran número de composiciones genéticas.
Por ello, cada uno tiene una composición genética especial, diferente a la de otros seres humanos, incluidos sus familiares (excepto el gemelo homocigótico).
Esto hace que cada ser humano tenga una combinación diferente y diferente de antígenos HLA. Y esta característica es la causa del rechazo vacunal entre los diferentes seres humanos, tanto abundante como gemela. Entre estas dos orillas hay una gran separación. En este periodo, a mayor paridad entre el donante y el receptor, mayor tasa de aceptación de la vacuna. Y viceversa.
Como puede deducirse de lo anterior, los autotransplantes (es decir, cuando el donante y el receptor son el mismo hombre) son un éxito total, ya que el Sistema Inmune del Hombre considera y acepta como propio el tejido insertado (figura 8).
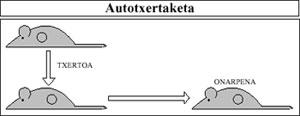
Se utilizan autocrecidos, por ejemplo, en pacientes que han sufrido grandes quemaduras de piel. En estos casos, las zonas quemadas del cuerpo se cubren con injertos de piel extraídos de las zonas sanas.
Mecanismos de rechazo
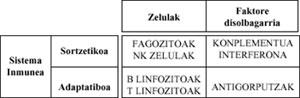
El Sistema Inmune tiene dos ramas: congénita e inespecífica y adaptativa o específica. Ambas ramas están formadas por células y factores solubles.
La primera, como su nombre indica, se excita desde el nacimiento y juega contra cualquier tipo de Ag.
La segunda, por su parte, se desarrolla a medida que el Sistema Inmune entra en contacto con moléculas extrañas (Ag) a lo largo de toda la vida humana, y sólo es opuesto a dichas moléculas (cuadro).
Como ya se ha mencionado, la causa del rechazo al trasplante es el Sistema Inmune Adaptativo del receptor, con ramas humoral (linfocitos B) y celular (linfocitos T).
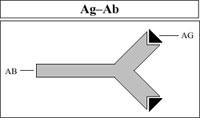
Los linfocitos B son células productoras de anticuerpos (Ab). Los anticuerpos son proteínas capaces de unirse a las moléculas extrañas (Ag) que originaron su producción (Figura 9).
De esta forma pueden producir diferentes tipos de respuesta inmune en sangre, sistemas linfáticos y mucosas del cuerpo.
Sin embargo, no cumplen grandes obligaciones en el primer rechazo vacunal, aunque son importantes en el segundo (si se produce). Esto se debe a que, tras el primer contacto con la vacuna extraña, los linfocitos B tardan varios días en producir anticuerpos, y cuando los producen, la vacuna ya ha sido rechazada por los linfocitos T, que actúan mucho más rápido.
Sin embargo, en la segunda vacuna recibida del mismo donante (si se recoge, claro está), los linfocitos B tienen preparados sus mecanismos de producción de anticuerpos y agreden más rápidamente la vacuna (recordar Figura 1). Sin embargo, rara vez se realizan vacunas con el mismo donante, por lo que el papel de los linfocitos B en los trasplantes es muy reducido.
Los linfocitos T, por el contrario, son las principales células causantes del rechazo vacunal. Estas células se distribuyen en cinco poblaciones, cada una de ellas con una función específica.

En el rechazo de trasplantes las poblaciones afectadas son dos: Los linfocitos T auxiliar (TH) y T citotóxico (TC). Los asistentes T tienen un receptor en la membrana para reconocer antígenos de la clase HLA-II (ver figura 4). Las T citotóxicas, por su parte, reconocerán los antígenos de la clase HLA-I (ver figura 5).
El mecanismo de rechazo del trasplante es el siguiente:
Reconocimiento: los auxiliares T del fermento ven de forma extraña las células de la vacuna a través de sus antígenos HLA-II.
1.
ayuda: Los ayudantes T estimulan las T citotóxicas mediante un factor soluble (linfocina).
citosis: Las T citotóxicas, por su parte, entran en contacto con las células de la vacuna (esta vez a través de los antígenos HLA-I) y realizan una acción de citotoxicidad o citosis contra ellas (Figura 10).
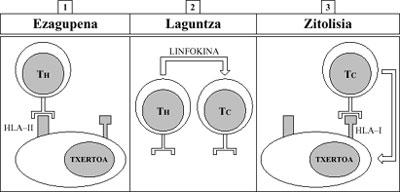
Esto provoca la muerte de las células de la vacuna, que son rechazadas.
Por tanto, cuando se rechaza el trasplante, este mecanismo natural, creado por sí mismo para destruir células propias pavimentadas o alteradas (mecanismo formado por los linfocitos HLA Ag y T), no cumple con su obligación original (Figura 5) sino una función artificial (los trasplantes son artificiales) (Figura 6).
Cómo evitar el rechazo
Emparejamiento Email-Receptor
Como ya se ha mencionado, existe una relación directa entre el número de inconformidades y el porcentaje de rechazo, es decir, cuando uno sube el otro y viceversa.
Aunque los alelos son muy variables y, por tanto, los genotipos humanos son diferentes, una forma de evadirse del riesgo de rechazo consiste en encontrar a un donante con el genotipo HLA lo más parecido posible al receptor.
Para ello se utilizan diversas pruebas, entre las que destaca el Tipaje Textil.
Mediante el Tipaje Textil se determinan las especificidades HLA de varios donantes, seleccionando la más compactativa con el receptor.
A pesar de que esta técnica es aplicable a familiares del destinatario, no es lo mismo aplicarla a donantes que no están relacionados con él por algunos inconvenientes.
Desgraciadamente, a pesar de la Tipificación Textil más atenta, siempre hay alguna inconformidad. Por lo tanto, la mayoría de las veces los médicos deben recurrir a la Inmunosupresión.
Inmunosupresión
La inmunosupresión, es decir, la supresión del Sistema Inmune del receptor, se puede conseguir por varios métodos. Entre ellas se pueden citar la irradiación, las drogas antimitóticas y el suero o sero antilinfocítico.
La irradiación del tejido linfoide del receptor elimina las células que realizan la acción citolítica, con lo que disminuye la fuerza del rechazo.
Las drogas antimitóticas impiden la proliferación linfocitaria del receptor, eliminando la respuesta inmune celular frente a los antígenos del donante. Las drogas más utilizadas son la ciclosporina A, la acatioprina y la ciclofosfamida.
Hoy son anticuerpos contra la TDT del destinatario. De esta forma se bloquean las células T y se reduce la capacidad de rechazo.
A pesar de que existen muchos medios para evitar o reducir el rechazo, ninguno es completo y peor aún, todos tienen inconveniente
Por ello, la solución completa para combatir el rechazo al trasplante sigue lejos. Los logros que se van a detectar en el futuro en esta materia parecen haberse conseguido estrechamente con los avances de la Inmunología.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian











