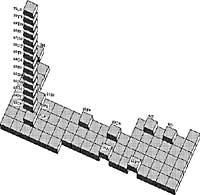
Tierras raras
Se denominan tierras raras a los 17 metales situados entre elementos químicos de número atómico 21 y 71, así como a los compuestos que los producen.
Estos diecisiete elementos son: Tres elementos del grupo III b [Escandio (Sc), Itrio (Y) y Lantano (La)] y la primera de las dos series, comúnmente denominadas lantánido, que se escriben fuera de la tabla periódica, compuesta por 14 elementos. El nombre de lantánido se debe a su descendencia. La serie de lantánidos se compone de: Cerio (Ce), Praseodimio (Pr), Neodimio (Nd), Prometio (Pm), Samario (Sm), Europio (Eu), Gadolinio (Gd), Terbio (Tb), Disprosión (Dy), Holmio (Ho), Blutitorio (Blu).
Historia
Nombre de tierra rara, XVIII. Desde el siglo XX, fecha en la que se realizaron los primeros descubrimientos sobre estos metales. La proporción de estos metales era mínima en aquellos minerales de los estudios iniciales. Ante esta escasez, estos investigadores creyeron que eran muy raros en la superficie terrestre. Posteriormente se ha podido comprobar que estaban equivocados. El cerio, el lantano y el neodimio son más abundantes en la superficie terrestre que el plomo. El itrio es más común que el estaño y la corteza terrestre es tan rica en tulios como en iodos.
La historia científica de estos elementos es muy turbulenta. La investigación de muchos años de dureza, mezcla y paso a paso tras el conocimiento acumulado hasta la actualidad. Entre el primer descubrimiento de un elemento de esta familia y el último en aislar pasaron 144 años. Tardó medio siglo en descubrir que el didimio era una mezcla de neodimio y praseodimio.
La larga historia de la investigación sobre tierras raras nació en 1794. Ese año el químico finlandés Johann Gadolin aisló el primer óxido de la familia de tierras raras. Aisló el óxido de una tierra rara de un mineral obtenido en el municipio sueco de Ytterby. Él creía que tenía un elemento nuevo que bautizó como iterbita. Finalmente, resumiendo, se llamó itria.
Años después, en 1803, investigadores como Martin Heinrich Klaproth o los famosos Jöns Jacob Berzelius, aislaron a la vez otra tierra rara, también óxido. Se le dio el nombre de Zeria en honor al recién descubierto asteroide Zere. Esto también fue un elemento puro. En 1808 Sir Humphry Davy demostró que las tierras raras descubiertas hasta entonces no eran elementos, sino combinaciones entre elementos metálicos y oxígeno. A los metales que aportaban óxidos de cería e itria se les denominaron cerio e itrio.
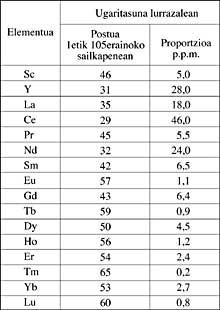
A lo largo de cuarenta años se consideró que la itria y la cería, es decir, las que se consideraban óxidos de itrio y de cerio, estaban químicamente bien definidas. Pero realmente eran mezclas de óxidos de tierras raras. En 1840 el mineralogista sueco Carl Gustav Mosander logró finalmente la división de la itria y la cería en tierras raras. Este fue el descubrimiento que abrió la puerta al camino hacia el aislamiento de toda la sucesión de tierras raras.
En los años posteriores se realizaron numerosas investigaciones, pero difícilmente se podía avanzar. Se crearon grandes confusiones en torno a ciertos descubrimientos, y con el fin de aclarar si éstos eran elementos puros o confusiones, se realizaron numerosas publicaciones. Los nombres de los elementos también cambiaban de laboratorio a laboratorio.
En 1869, cuando el químico ruso Dimitri Ivanovitx Mendeleiev propuso la tabla periódica, previó la necesidad de dejar un hueco para el escándo. En 1871 también prevé algunas características de este elemento. Cuando en 1879 se descubrió el esquandio y se informó de sus características se observó que se ajustaban a lo previsto por MendeleiEV. Este hecho provocó que la tabla de Mendeleiev fuera aceptada entre los científicos.
Las investigaciones prosiguieron con dureza, lo que permitió aislar la lutecio en 1907, último elemento de la serie.
Pero la verdad es que el elemento prometio no se aisló hasta mucho más tarde. Cuando Henry Moseley asignó a cada elemento de la Tabla Periódica un número atómico, se pudo conocer exactamente dónde estaban los agujeros libres. Hasta los años 1913-14 y Moseley descubrió que los lantánidos sólo podían ser 14 (desde el cielo hasta la lutecia) y que el número atómico 61 era el único que todavía estaba por descubrir. Sin embargo, no se aisló hasta 1947. Se le denominó Prometio.
¿Por qué ha sido tan difícil identificar y aislar estos elementos? La razón puede estar en que estos elementos se encuentran en un mismo mineral y presentan características químicas muy similares. Por eso han estado escondidos durante tanto tiempo. Lo más lantánido es el grupo de elementos con características más similares. Analizando un metal dado por puro en un descubrimiento con las nuevas técnicas desarrolladas en los próximos años, en más de una ocasión se pudo comprobar que era una mezcla de dos o tres tierras raras.
Una ventaja de tener propiedades químicas tan similares es que, en el uso industrial, cuando se deben aprovechar estas propiedades, no merece la pena una distribución muy fina. Esta distribución resulta necesaria cuando las características a aprovechar son características físicas.
Estructura electrónica
A continuación veremos cómo están dispuestos los electrones de estos elementos. Se sabe que los electrones se disponen en capas alrededor del núcleo del átomo. A cada capa le corresponde un número cuántico n y para los lantánidos n = 6. Cada capa tiene un determinado número de electrones y éstos están organizados a su vez en subcapas. Estas subcapas son "s", "p", "d" y "f".
A medida que aumenta el número atómico, el número de electrones también aumenta. A la estructura electrónica del elemento anterior se le añadirá un nuevo electrón por el que se relaciona a continuación. El electrón añadido no se ubicará en cualquier lugar. Una serie está formada por el conjunto de elementos que corresponden al número de electrones necesarios hasta completar una subcapa en formación.
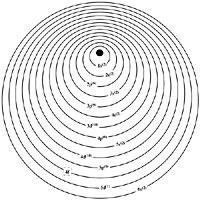
Los electrones más estables son los electrones "s" y "p", por lo que tienden a situarse en estas primeras subcapas. Al finalizar el quinto período de la Tabla Periódica, las subcapas 4s, 4p, 4d y 5s y 5p están completas. El sexto período comienza con la incorporación de dos 6s electrones y el tercero va al orbital 5d formando el elemento denominado lantano. El cuarto electrón se dirige a la subcapa 4f, hasta entonces vacía. Dado que esta subcapa tiene capacidad para 14 electrones, la serie está compuesta por 14 lantánidos, desde el cero hasta el lutecio.
El itrio y el escandio que forman la familia de las tierras raras se encuentran en la misma columna de la tabla periódica en la que se encuentra el lantano. Los electrones más superficiales del escandio son dos electrones 4s y un electrón 3d. En el caso del itrio, los electrones 5s y 4d.
Primeros usos de tierras raras
El cerio fue el primero que ganó fama y fama entre las tierras raras y que en cierta medida provocó investigaciones hasta conocer a toda la familia.
El descubrimiento realizado por el barón Auer von Welsbach en 1883 está en la base del interés que suscitó el cielo. El barón publicó ese año un nuevo método de iluminación. Welsbach mojaron un tejido en disolución de sales de torio, cerio y otras tierras raras. A continuación descubrió que el tejido da luz brillante poniéndolo en calor de una llama de gas. Era un descubrimiento muy sorprendente para esta época. Se trata de una característica que todavía se utiliza en la actualidad, ya que es el modo de funcionamiento de la camisa refractaria de las lámparas de gas del camping.
Años después, en 1903, el propio Auer von Welsbach descubrió otro uso de tierras raras: la piedra mechera. El cerio es un piroforo, es decir, tiene la facilidad de inflamarse espontáneamente en el aire y de sacar chispas frotando. El cerio tuvo que ser aleado con hierro para usarlo en piedras de mechero, de manera que no se alimentaba del fuego. Este es el primer paso que se dio para utilizar tierras raras en metalurgia.
Una característica común a estos dos usos es que no requieren elementos de gran pureza. Por ello, se pudieron explotar industrialmente en aquellos tiempos en los que los métodos de distribución química para estos usos no estaban tan desarrollados.
Usos industriales actuales
Metalurgia

Entre 1960 y 1974 una aleación denominada mischmetal, compuesta por lantanos, cerios y neodimios, experimentó un espectacular auge en los procesos de fundición y purificación del acero. Debido a la afinidad de esta aleación con el oxígeno y el azufre, es adecuada para su uso como desoxidante y desulfurante. Mejora las propiedades anticorrosivas.
En el hierro fundido, los materiales son más resistentes, dúctiles y por tanto más fáciles de procesar.
En la actualidad se reduce el uso de este mischmetal al aumentar el uso de compuestos de calcio en la desulfurización.
Reacciones catalizadas
Las tierras raras están muy extendidas en reacciones químicas como la polimerización o la hidrogenación, que sirven para acelerar o modificar. Los lantánidos raramente actúan como auténticos catalizadores, siendo su papel asegurar la estabilidad, activación y selectividad del sistema catalítico.
En el cracking del petróleo, por ejemplo, se utilizan como catalizadores estructuras cristalinas denominadas zeolitas. Están constituidos por silicio y aluminio y elementos alcalinos como potasio y sodio. La sustitución del sodio por una mezcla de tierras raras mejora las características catalíticas y la vida efectiva de la zeolita.
Bote catalítico de vehículos
Los catalizadores se utilizan en el bote catalítico para estabilizar, optimizando su funcionamiento y alargando su vida. Los potes catalíticos se obtienen mediante la aplicación de componentes activos (platino, paladio y rodio) en una estructura similar a las celdas de abeja formadas por aluminio y óxidos de cerio o lantano. En los países con legislación anticontaminación más exigente, el uso del bote catalítico es absolutamente necesario, lo que significa que se necesitan cientos de toneladas de tierras raras anuales.
Vidrio y cerámica
La industria del vidrio y la cerámica es uno de los mayores consumidores de tierras raras. Las tierras raras absorben y emiten selectivamente varias longitudes de onda del espectro visible y ultravioleta. Por tanto, los colores obtenidos son muy claros, muy definidos y estables. Por ello, las tierras raras se utilizan como colorantes e incluso como luminoforos.
Aunque parezca lo contrario, las tierras raras también se utilizan para obtener vidrio incoloro. Añadiendo a un vidrio rojo una extraña tierra que absorbe selectivamente el rojo, se obtiene un vidrio incoloro que reequilibra el espectro de colores.
Los vidrios con tierras raras soportan muy bien la luz solar, por lo que se utilizan no sólo para ventanas sino también para gafas de sol.
Pantalla de TV en color
Como ya se ha mencionado anteriormente, el primer uso industrial del óxido de cerio fue el mechero de Welsbach, como dicen Auer, u otros. Sabemos que lo que está por debajo de este uso es una característica que se convierte en luminiscente con el calor. Este resultado era extremadamente sorprendente en aquellos tiempos, por lo que surgió un gran interés entre científicos y no científicos sobre tierras raras. Pero ha sido necesario esperar hasta la década de los 60 para poder dar valor a esta propiedad física.
Para entonces, vamos a tener en cuenta que para la década de los 60 los métodos de distribución química estaban mucho más desarrollados y apareció una televisión de colores. Los luminoforos, es decir, los aspectos sensibles del tubo catódico, además de tener una buena luminosidad y una larga duración, deben dar un color muy bien definido. Dado que el vanadato del itrio activado por Europa cumple estos requisitos, se utiliza en pantallas de TV en color.
Estas son las características que justifican el uso del europio en la iluminación fluorescente.
Imanes permanentes
En 1969 los investigadores descubrieron que con la introducción del samario en una aleación de cobalto se obtenía un imán duradero extremadamente poderoso. Este imán es muy resistente a la desimantación y es 30 veces más fuerte que los imanes tradicionales y seis veces más fuerte que las ferritas (los mejores imanes de la hora).
Con las tierras raras se pueden conseguir imanes mucho más pequeños que tienen la misma fuerza y así podemos llegar al Walkman del ditxoso, tan conocido en la actualidad. Las ventajas que ofrecen los imanes de samario y cobalto son tan elevadas que se utilizan en la mayoría de los electroimanes de motores de baja y media potencia, aunque su precio sea muy elevado.
Con el objetivo de superar la barrera del precio, se han realizado más investigaciones y en 1983 se ha detectado que los imanes compuestos por ferboros y neodimios tienen las propiedades adecuadas. De esta forma se puede evitar el uso de un metal tan caro como el samario. Este nuevo material no mantiene sus características por encima de los 300ºC (mientras que el samario-cobalto los mantiene hasta los 700ºC), lo que dificulta su uso para ciertas funciones como los motores de arranque de vehículos.
Por superconductividad

La superconductividad consiste en la desaparición de la resistencia eléctrica y por tanto de la disipación energética. Muchos materiales presentan esta propiedad cerca del cero absoluto (-273ºC).
En los estudios de los últimos años se han encontrado materiales que presentan esta propiedad a temperaturas superiores. En 1986, un óxido de lantano, bario y cobre fue hallado como superconductor a -243ºC. A. Müller y J.G. Los físicos alemanes Bednorz. Por este trabajo recibieron el Premio Nobel y abrieron una nueva etapa en el campo de la superconductividad a temperaturas más altas.
Los nuevos estudios llevaron el límite hasta -183ºC con óxidos ternarios con tierras raras. Hoy en día el récord ha alcanzado los -148ºC y nadie sabe hasta qué punto los investigadores podrán llevar esta limitación en los próximos años.
Los usos mencionados no cierran la lista. La radiología, los láseres, la óptica de ajuste y la joyería son campos que aprovechan las propiedades de las tierras raras.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian