Un embryon, une grossesse
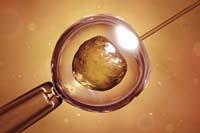
À l'hôpital Quirón de San Sebastián, la docteur Miren Mandiola est présente devant neuf embryons. Ce sont des embryons qui survivent après trois jours. Une femme qui ne pouvait pas avoir d'enfants a été enlevée de quinze obocytes après avoir stimulé ses ovaires avec des hormones. Mandiola a introduit un spermatozoïde à chaque ovocyte par micro-injection. Car neuf de ces quinze embryons ont avancé. Et maintenant, vous devez choisir trois de ces neuf pour s'imposer à la femme. Ce n'est pas une décision quelconque, puisque la probabilité d'obtenir la grossesse dépend de la qualité de l'embryon.
Mandiola sélectionne embryons en tenant compte de plusieurs caractéristiques: "Nous avons choisi selon des critères morphologiques". Un critère est la vitesse de croissance: "l'ovocyte fécondé avec le spermatozoïde doit avoir quatre cellules à 48 heures, c'est le stade parfait et à 72 heures le stade parfait est de huit cellules". Ils font une sorte de score pour mesurer la qualité morphologique. Il existe un certain nombre de caractéristiques morphologiques qui indiquent une bonne ou mauvaise évolution de l'embryon. Si vous avez plus ou moins de cellules nécessaires, il ne convient pas; si les cellules ne sont pas de la même taille, vous n'avez même pas de parties de détritus. Deux ou trois embryons sont choisis avec le plus grand score, sachant que ce sont ceux qui ont la plus grande capacité d'adhérence à l'utérus ».
Mais les embryons de bon aspect ne doivent pas être sains. « Nous transférons beaucoup d'embryons de bonne apparence, mais il reste très peu de femmes enceintes », explique Mandiola. Certains de ces embryons peuvent subir des mutations dans des gènes ou des aneuploïdes, à savoir un nombre anormal de chromosomes. Dans de nombreux cas, les embryons ne collent pas ou ne produisent pas d'avortement en moins de trois mois. La seule façon de rejeter ces embryons est aujourd'hui d'effectuer un diagnostic génétique, le diagnostic génétique préimplantatoire (DGP).
Mais le diagnostic génétique n'est pas toujours réalisé dans des cas concrets. Par exemple, dans les familles avec une maladie génétique grave, pour choisir des embryons sans maladie. La maladie de Huntington, la fibrose kystique ou la dystrophie musculaire de Steinert, par exemple. Le DGP est également réalisé lorsque la femme a subi des avortements répétés, car l'origine des avortements peut être dans la quantité ou la structure anormale des chromosomes des embryons.
Le DGP consiste à extraire une cellule à l'embryon, il s'agit donc d'une technique invasive. "Manipuler l'embryon n'est pas bon, bien sûr", raconte Mandiola, "moins il touche, mieux, plus il sera viable. Cependant, les techniques utilisées pour l'élaboration du DGP sont généralement celles qui permettent à l'embryon d'avancer avec une bonne capacité de développement. Le DGP doit donc être réalisé dans le stade approprié de l'embryon, avec 6 à 8 cellules. De cette façon, l'embryon est capable de continuer à croître, même s'il fait un trou et retire l'une des cellules".
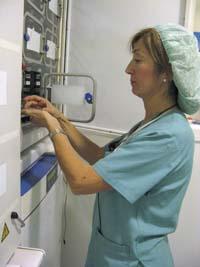
Sur la courroie des embryons
Les embryologistes apprécieraient une technique rapide, simple et non invasive qui les aiderait à choisir des embryons sains. Mais aujourd'hui, il n'y a pas. Embryomics s'y efforcent en analysant les métabolites du milieu de culture embryonnaire pour obtenir des informations sur la santé des embryons. Cette recherche appartient au domaine de la métabolomique. Pour Francisco Dominguez, d'Embryomics, « la métabolomique fournit aux embryologues et gynécologues des informations biochimiques qui les aident dans le choix des embryons ».
Les métabolites sont les molécules apparaissant dans le métabolisme de l'embryon, qui les attrape du milieu d'alimentation des embryons, ou qui les élimine comme résidus. Le glucose, le piruvate, le lactose, par exemple, sont des métabolites.
Embryomics naît dans le contexte de la fécondation assistée par la Fondation IVI de Valence. Il s'agissait d'un projet de recherche à l'origine qui, compte tenu de son succès, se sont déplacés à la Biokabia du Parc Technologique de Biscaye, centre de création d'entreprises de biotechnologie. Ils explorent les moyens de croissance des embryons fabriqués par DGP d'Embryomics. Ils peuvent ainsi assimiler l'étude métabolomique du milieu au résultat du DGP, c'est-à-dire comparer les profils de métabolites d'embryons normaux et anormaux.
Selon Domínguez, « les embryons et normaux avec beaucoup d'anomalies chromosomiques se distinguent à 100% selon le profil des métabolites. Dans d'autres cas, la séparation est moins claire, par exemple, quand il n'y a qu'une seule monosomie - au lieu d'une paire de chromosomes - il y a un chromosome unique - il est plus difficile de trouver des différences, car elle est plus proche de l'embryon normal, mais elles se distinguent également dans ces cas".
Pour réaliser cette séparation, plus de mille métabolites sont analysés. « Ce sont des échantillons très complexes, le métabolisme a beaucoup de métabolites et nous analysons au maximum », explique Domínguez. « Nous connaissons certains de ces métabolites, mais la plupart d'entre nous les ont non identifiés, nous les différencions simplement par masse et temps de rétention ». Ils utilisent l'imagerie par résonance magnétique et la spectroscopie de masse. Ces techniques permettent de mesurer des concentrations très petites. Mais l'équipement est très cher et il faut des gens formés. C'est pourquoi Embryomics travaille avec Owl Genomics, qui apporte des ressources techniques et son expérience en métabolomique. Ce centre est également situé dans le parc technologique de Biscaye.
Un projet, pour le moment
Domínguez espère que les résultats seront publiés pour la fin de l'année, mais il veut préciser: "C'est un projet et pour le moment nous sommes en phase de recherche, mais nous développons le produit et au moins au début nous l'offrirons aux cliniques IVI". L'offre sera un service. Dans le laboratoire, on ramassera les moyens cultivés par l'embryon (gouttelettes d'environ 40 microlitres) et on les enverra à Embryomics, obtenant le résultat en 24 heures. Cela permettra à l'embryologiste de mieux différencier les embryons normaux des non-normaux.

Ce sera un outil de plus pour l'embryologiste. Selon Mandiola, "probablement dans quelques années la métabolomique aura une application clinique claire. Mais il est encore un peu vert. Et d'ailleurs, la métabolomique dira quel embryon adhèrera plus facilement d'un point de vue chromosomique. Il servira pour les cas normaux, pour les fécondations in vitro conventionnelles. Mais pas pour remplacer le DGP. Dans le DGP, vous devez être clair sur ce que vous cherchez".
Esther Fernández coïncide avec Mandiola. Cet embryologiste, un des pionniers dans l'élaboration de DGP en Espagne, considère que la métabolomique peut avoir beaucoup d'applications dans l'embryologie humaine, mais ne sera pas du tout substitut au DGP. Il explique que, entre autres, « le diagnostic génétique préimplantatoire (DGP) est utilisé dans les embryons de couples porteurs d'une maladie grave, ainsi que dans le diagnostic de certaines maladies génétiques ou d'altérations chromosomiques – les deux héréditaires –. Et ce DGP ne pourra jamais être remplacé par la métabolomique ».
Cependant, Fernández voit dans la métabolomique un rôle important dans l'un des grands défis de l'embryologie : le transfert d'un embryon unique. Quand l'embryologiste est sur le point de choisir parmi plusieurs embryons, en plus du score morphologique, il aurait une autre donnée pour choisir la meilleure option.
Cependant, aujourd'hui, comme l'explique Mandiola, le nombre de grossesses est faible, par rapport au nombre d'embryons implantés (40%-50%), de sorte que deux ou trois embryons sont transférés à la mère dans chaque cycle, dans la mesure du possible. Cela suppose un risque de grossesses multiples, et la grossesse de jumeaux – et surtout de triplés – est un risque inhérent tant pour la mère que pour les enfants. Par conséquent, l'idéal serait de transférer un embryon unique, donc il faut beaucoup de sécurité que cet embryon avance. En cela consiste donc le grand défi de la métabolomique: être un outil pour choisir l'embryon le plus viable.
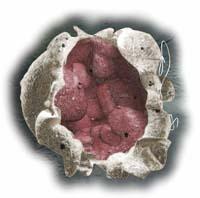
L'équation d'un embryon égal à une grossesse, pour le moment, est loin de la réalité. Au laboratoire, Mandiola a sélectionné les trois meilleurs des neuf embryons et, dans la salle d'opération, les ont transférés à la femme. Il ne reste qu'à attendre que l'un d'eux colle maintenant.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian














