Autorización para iniciar sesións clínicas para un medicamento de esclerose lateral amiotrófica
A Axencia Española de Medicamentos e Produtos Sanitarios (AEMPS) autorizou que se probe en persoas un fármaco que poida ser eficaz para a esclerose lateral amiotrófica (ELA). O fármaco, denominado AP-2, foi desenvolvido no Centro de Investigacións Biolóxicas Margarita Salas do CSIC. Está previsto que as probas comecen en abril. En primeiro lugar, avaliarán a seguridade e a farmacocinética en voluntarios sans e esperan iniciar a seguinte fase cos pacientes en xaneiro de 2027.
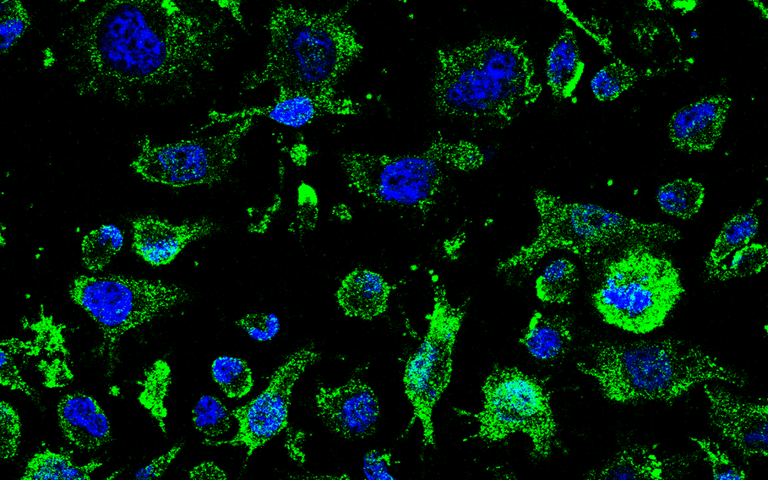
A finalidade do fármaco AP-2 é a readquisición da función da proteína TDP-43. A proteína TDP-43 está modificada patológicamente en pacientes con EEA e causa a morte de neuronas motoras, as células do sistema nervioso encargadas de transmitir sinais desde o cerebro ou a medula espiñal aos músculos. O fármaco AP-2 logrou reverter a anomalía do TDP43 tanto en modelos celulares como en animais transxénicos.
«A proteína TDP-43 está modificada patológicamente en pacientes con AEA e causa a morte de neuronas motoras»
Os investigadores afirman que, aínda que aínda é pronto, a reprodución dos resultados en células e animais podería retardar a enfermidade e, no mellor dos casos, freala.
En Europa só existe un fármaco aprobado en Europa para o tratamento da ELA: o riluzol, un fármaco paliativo que mellora a sintomatología e alarga a esperanza de vida entre tres e seis meses. Por tanto, a autorización do ensaio clínico da AP-2 é un avance esperanzador.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian