Pharmacies vivantes

Il y a un an, l'Agence européenne des médicaments (EMEA) a autorisé la commercialisation pour la première fois dans le monde d'un médicament produit par un animal transgénique. Plus précisément, il a autorisé l'utilisation de la protéine ATryn produite dans le lait par chèvre génétiquement modifiée. Cette protéine, produite par GTC Biotherapeutics, est une antitronbine humaine, anticoagulante. Empêche la formation de coagines chez les patients présentant une carence de cette protéine.
Quelques mois plus tôt, l'agence n'a pas autorisé cette antitronbine parce qu'elle a été testée dans des tests cliniques chez très peu de patients. Mais le manque d'antitrobine est une maladie rare, seulement un sur 3.000 et 5.000 personnes souffrent, il n'est donc pas facile d'obtenir de nombreux patients volontaires. Cependant, il a ensuite été décidé que les tests présentés par GTC étaient suffisants. Parmi les volontaires se trouvaient également des femmes enceintes, et les experts ont montré que l'antitronbine est totalement sûre et a la même efficacité chez les femmes non enceintes et enceintes.
En plus de la société GTC, d'autres sociétés génératrices de substances thérapeutiques chez les animaux transgéniques ont pris la nouvelle avec espoir. Ils espéraient depuis longtemps ouvrir les portes du marché et ont tout de suite vu la conclusion du passage de la SAME: La valeur marchande de GTC a augmenté de plus de 20% et celle de sa concurrence voisine, la société Pharming, a augmenté de près de 10%.
En outre, deux semaines après son autorisation sur ATry, la SAME a autorisé la commercialisation d'un anti-inflammatoire produit par Pharming par des lapins transgéniques. On pensait que derrière cela allaient aller d'autres.
Ce n'est pas le cas. Et c'est qu'ils doivent s'assurer que les sujets créés sur les animaux transgéniques sont sûrs et pour cela ils doivent surmonter beaucoup de tests. En particulier, ils doivent tenir compte de quatre points: réponses allergiques, réponse du système immunitaire, réponse auto-immune et infections, y compris celles provoquées par des prions. Pour garantir et prouver qu'ils sont sûrs de toutes les parties, ils doivent utiliser une technique très avancée et présenter de nombreux tests. Et pour cela, il faut beaucoup de temps et d'argent.
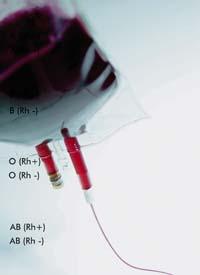
Laits très spéciaux
Il y a dix ans, cependant, on ne connaissait pas les inconvénients et beaucoup de chercheurs attendaient beaucoup dans ce domaine. En 1996, l'Institut Roslin a présenté Dolly, le premier animal cloné d'une cellule adulte. Un an plus tard, dans le même institut, naissent deux autres moutons clonés, Molly et Polly. Ils ne ressemblaient pas beaucoup à Dolly, mais se caractérisaient par avoir dans leur génome un gène humain.
Ce gène codifie la protéine appelée facteur IX. C'est une protéine coagulante de sang qui est utilisé pour traiter l'hémophilie, qui est ce qui leur manque dans le sang. Mais la seule source pour obtenir le facteur IX est le plasma sanguin des humains et pour cela ils ont créé Molly et Polly pour créer un troupeau de moutons qui a apporté le facteur IX dans le lait. Cela signifierait un marché important de cette protéine.
Par conséquent, pour produire des molécules biologiques comme des protéines, des anticorps, l'ingénierie génétique a semblé une grande occasion. Jusqu'alors, on utilisait des cultures cellulaires de micro-organismes, de levures ou d'animaux ou de personnes, et c'est la voie principale. Cependant, c'est une méthode difficile et coûteuse, dans laquelle les molécules produites dans les cultures exigent des changements complexes pour pouvoir être utilisées en thérapie, obtenant en outre de petites quantités. Par conséquent, ils considéraient que la transformation des animaux en producteurs de médicaments pourrait englober le produit.
Par conséquent, ils ont essayé de le faire. Molly et Polly n'ont pas atteint leur objectif, mais les chercheurs ont continué à travailler avec des vaches, des moutons et des chèvres. En fait, ces animaux sont utilisés pour produire du lait, et si grâce à l'ingénierie génétique, ceux-ci et leurs descendants parviennent à former des molécules humaines dans le lait, il suffit d'isoler les protéines du lait.

Sur ce chemin, le travail effectué par la société GTC avec chèvre a porté ses fruits et on estime que l'obtention d'antitronbine par chèvre transgénique est entre 30 et 100 fois moins cher que la production dans les cultures cellulaires.
Les vaches produisent plus de lait que les chèvres, donc elles ont été sélectionnées par Advanced Cell Technology. Dans le lait des vaches transgéniques on prétendait obtenir la protéine séroalbumine du sang humain. La séroalbumine est utilisée pour augmenter le volume de sang, par exemple chez les patients souffrant de blessures traumatiques. On considérait que le lait de vache pouvait être une source imbattable, car une seule vache peut apporter plus de 8.000 litres de lait par an, ce qui pourrait représenter entre 40 et 80 kilos de protéines.
Cependant, ce domaine n'a pas été le développement prévu. De nombreux projets sont en cours de route et, bien qu'actuellement le marché de ces molécules pour la thérapie déplace 24.500 millions d'euros, les produits produits à partir d'animaux génétiquement modifiés continuent d'occuper une part très réduite.
Œufs et plantes
Cependant, les chercheurs ne se rendent pas et maintenant ils veulent également produire des protéines humaines d'utilité médicale dans les oeufs. La méthode est similaire à celle utilisée dans les ruminants. Comme les ruminants dans le lait, les poules génétiquement modifiées produisent des protéines thérapeutiques dans les œufs.

La culture des poulets transgéniques présente certains avantages par rapport au bétail. Ils sont bon marché, productifs (chaque poule peut pondre 300 oeufs par an) et la distance intergénérationnelle est petite. Cela facilite l'adaptation de la production à la demande.
L'Institut Roslin, en collaboration avec Viragen et Oxford Biomedica, a réussi à produire deux protéines thérapeutiques dans la clairière des œufs de poules transgéniques. L'un d'eux est l'anticorps Mini-R24, prétendument utile contre le mélanome malin, et l'autre interféron b-1 humain, utilisé pour traiter la sclérose en plaques et d'autres maladies. La recherche, publiée cette année dans le magazine scientifique PNAS, vise à poursuivre les recherches pour améliorer les résultats.
Cependant, en plus des poules, les ruminants ont d'autres concurrents: les plantes. Les chercheurs ont depuis des années pour que les plantes aient des caractéristiques qui veulent transformer génétiquement, notamment la capacité de produire des protéines humaines et des vaccins.
Les plantes transgéniques sont plus faciles à cultiver que les animaux et ont également moins de risque d'infection par virus ou prions. Au contraire, ils provoquent plus d'allergies et, surtout, ont un risque élevé de s'étendre à l'environnement. En fait, pour beaucoup de gens, c'est l'une des principales raisons d'être contre les OGM. Par conséquent, les fabricants sont tenus de prendre des mesures drastiques pour éviter ce risque.
Par exemple, des chercheurs de l'Université Purdue US cultivent des plantes transgéniques dans une mine située dans l'Indiana. Cela garantit que les plantes extérieures ne seront pas affectées. Ils étudient avec du maïs, du tabac, de la luzerne et du soja, entre autres, pour créer des anticorps, de l'insuline et des vaccins.

Il existe de nombreuses études de plantes transgéniques capables de produire ce type de molécules, et récemment le Département américain de l'agriculture. a reçu l'autorisation de cultiver du riz qui produit des protéines qui se trouvent dans le lait féminin. Le riz transgénique contient du lysozyme, de la laktoferrine et de la séroalbumine humaine. La lysozyme et la laktoferrine ont des propriétés antibactériennes, virales et fongiques, et avec le riz, les chercheurs veulent élaborer une boisson pour traiter la diarrhée et l'anémie.
Malgré les problèmes, les animaux et les plantes génétiquement modifiés deviennent une source de molécules thérapeutiques. Cependant, ils sont encore à ses débuts, tandis que l'efficacité des systèmes de génération de ces molécules dans les cultures cellulaires augmente. Le temps dira quelle est la meilleure voie, pour l'instant les chercheurs ne veulent pas fermer la porte.


Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian











