Inmunoterapia CAR: una puerta a la esperanza

La oncohematóloga Izaskun Zeberio Etxetxipia habla con orgullo sobre su obra. Tras su investigación y trabajo en el Hospital de Navarra y en el Centro de Cáncer Memorial Sloan-Kettering (Nueva York), desde 2014 se encuentra en el Hospital Universitario de Donostia. Es el referente de la Unidad Linfoma y explica que prestan atención diurna a pacientes sin ingreso: “Procuramos evitar el ingreso ya que para el paciente es mucho más agradable y tierna”.
Es testigo directo de la evolución que está experimentando en los tratamientos y vive de primera mano la puerta abierta por la inmunoterapia. Explica que el tratamiento clásico es la quimioterapia: “Para comprenderla fácilmente, las células cancerosas son células que se reproducen más de lo suficiente y no mueren, y la quimioterapia corta el ciclo celular”.
En inmunoterapia el foco es otro: en lugar de poner la fuerza en la destrucción de la célula cancerígena, se coloca en el refuerzo o aumento del sistema inmunitario. “Precisamente a eso le dieron el Premio Nobel de Medicina de 2018”, ha recordado Zeberio. “Gracias a estos estudios sabemos que las células tumorales se ocultan para evitar que el sistema de vigilancia del sistema inmunitario detecte y destruya. Envían una señal para crear una zona de protección y entregaron el Premio Nobel a aquellos que desarrollaron anticuerpos monoclonales que bloqueaban esas señales”.
Hoy en día se siguen utilizando anticuerpos monoclonales pero, además, las células CAR han adquirido una gran fuerza: “Han despertado una gran esperanza. Una esperanza basada en evidencias, no demasiado”, ha afirmado.
Según él, llevan más de veinte años investigando con células CAR y se han realizado numerosos ensayos clínicos, sobre todo en EEUU y China, que ya han llegado a la clínica: “Desde hace un año es posible aplicar esta terapia en el sistema sanitario público”.
El núcleo es una quimera
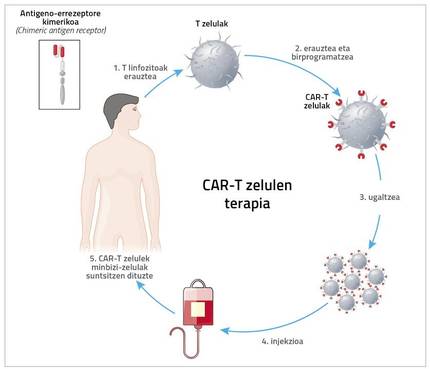
El acrónimo CAR significa chimeric antígeno receptor receptor químico. Para ello se extrae al paciente unas células del sistema inmunitario. “Normalmente se trata de células T, por lo que se denomina terapia CAR-T. Pero se puede hacer con otras células, como las NK. Cristina Egizabal Argaiz, del Centro de Transfusiones y Tejidos Humanos de la Comunidad Autónoma del País Vasco, está realizando con ellos estudios muy interesantes”, explica Zeberio.
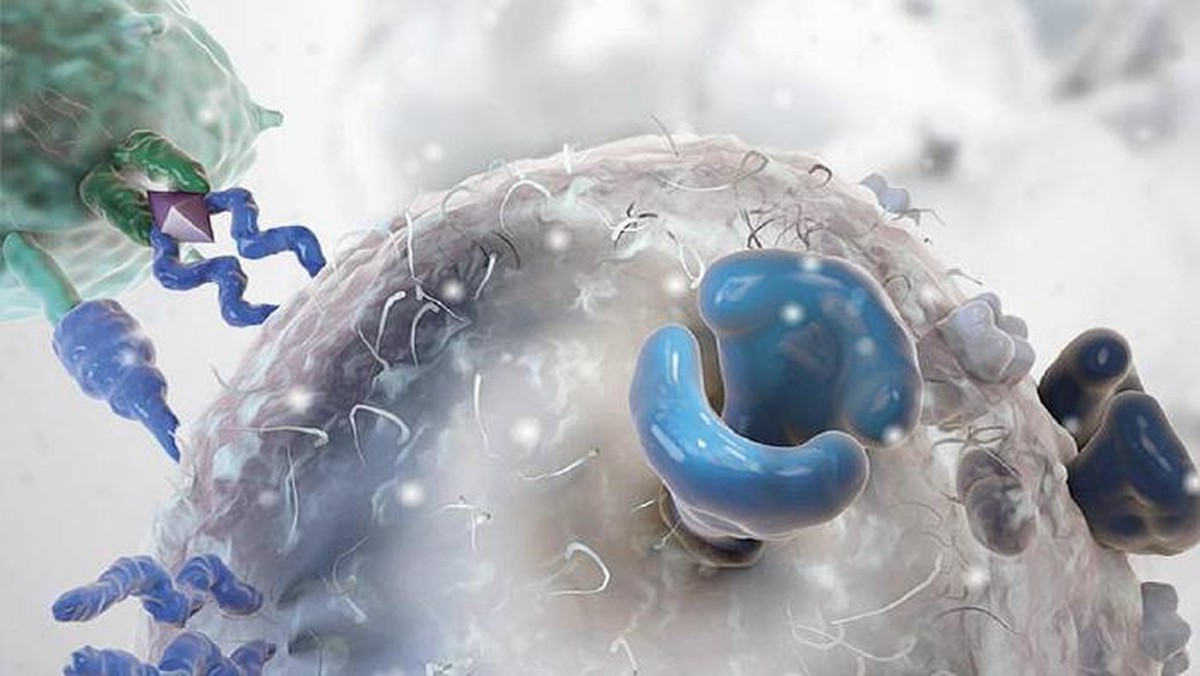
Sin embargo, lo que de momento ha llegado a la aplicación clínica es la terapia de células CAR-T. Por tanto, al paciente se le extraen las células T y, mediante un proceso muy complejo y caro, se introduce un nuevo receptor a esta célula T. Gracias a este receptor, la célula T tiene una gran capacidad de detección y destrucción de antígenos de células cancerosas.
Y de ahí el nombre. Zeberio: “Kimera es un monstruo de la mitología griega formado por fragmentos de cabra, león y dragón. Pues bien, en el receptor quimérico se realiza una mezcla de linfocitos B y T. La parte del linfocito B detecta el antígeno y la del linfocito T penetra en la célula y da señal de activación y reproducción”.
Esta tecnología se puede diseñar para diferentes antígenos. Zeberio indica que en hematología predomina un antígeno, el CD19, por lo que las células CAR-T que se utilizan son anti. “Por tanto, el mayor desarrollo y los mejores resultados se han obtenido en los cánceres de la línea B donde se expresa el antígeno CD19. Especialmente en la leucemia aguda linfoblástica, es decir, en la leucemia infantil. Además, todos los linfomas no Hodgkin B (90% de los linfomas que tratamos) expresan el CD19”.
De la investigación a la clínica
En base a los resultados de los ensayos clínicos, en 2017 la Agencia Estadounidense de Alimentos y Medicamentos, FDA, aprobó el uso comercial de las células CAR-T y fue aprobada un año después por la Agencia Europea de Medicamentos, la SEM. En España, desde noviembre de 2018 es posible utilizar la terapia en los centros.
“Es muy importante elegir bien a los pacientes que realmente se benefician”, advierte Zeberio. “Es cierto que ha generado unas expectativas muy elevadas, ya que estos pacientes no tienen otra alternativa, pero hay que tener en cuenta que hay que tener en cuenta que hay que elegir bien a aquellos pacientes a los que les va a beneficiar el tratamiento, porque el procedimiento es muy complicado, muy caro y puede tener efectos secundarios graves. No es para todos los pacientes y tenemos que decidir con mucho cuidado a quién entregarlo”.
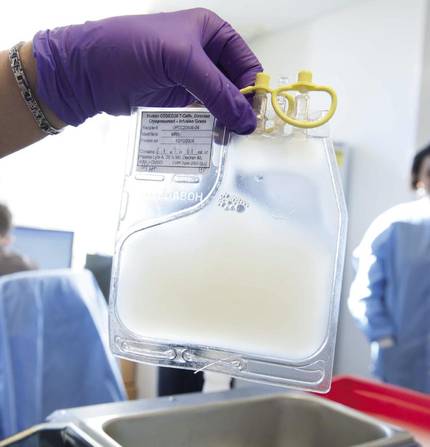
“Además, no hay que olvidar que la terapia tiene efectos secundarios significativos”. De hecho, al paciente primero se le extraen los linfocitos T y se envían a EEUU. Allí, mediante unos retrovirus o lentivirus, introducen un receptor a los linfocitos. Luego se reproducen en el laboratorio y son enviados de vuelta. Mientras tanto, pueden transcurrir 5 semanas en las que hay que analizar cómo tratar al paciente. Una vez llegadas las células se incorporan al paciente.
Cuando recibe a los pacientes, Zeberio explica que hay toxicidad durante las dos primeras semanas: “Por ello, el paciente debe estar en buen estado. Hay que tener en cuenta que existe una lucha entre los linfocitos T que ha recibido y las células cancerosas y otras células del paciente. Se produce una tormenta de citoquinas que puede provocar shock e insuficiencia respiratoria. Entonces hay que atender al paciente en cuidados especiales”.
No es de extrañar, por lo tanto, subrayar que deben actuar con responsabilidad. “No hay que olvidar que esta terapia se aceptó con muy pocos casos. Dado que sus resultados son tan satisfactorios en pacientes que no tienen otra alternativa, ha saltado muy rápido de los ensayos de los investigadores a la práctica hospitalaria, pero debemos medir con rigor la seguridad y la eficacia. De alguna manera es como si estuvieran en la 3ª fase clínica”. En definitiva, la prioridad es curar a los pacientes, pero al mismo tiempo están aprendiendo y mejorando.
Además de la tormenta de citoquinas, puntualiza que a veces se produce neurotoxicidad. Todavía no entienden muy bien el mecanismo, pero hay pacientes que sufren neurotoxicidad, desde la confusión, hasta la dificultad de escribir o hablar, pasando por el coma. Para hacer frente a estos riesgos es evidente que el paciente debe estar fuerte en el momento de recibir los linfocitos modificados.
Dice Zeberio: “Los médicos debemos medir beneficios y riesgos, y sólo aplicaremos el tratamiento si el beneficio es mayor que el riesgo. No para todos”.
Criterios estrictos, plan detallado
En España, el Plan de Terapias Avanzadas establece los criterios para la implantación del tratamiento CAR-T. El objeto del citado plan es, literalmente, el siguiente: Organizar de forma planificada, equitativa, segura y eficaz el uso de los medicamentos CAR y actualmente de los CAR-T en el sistema sanitario público, así como su investigación y producción en el ámbito académico del sistema sanitario público en condiciones que garanticen estándares de calidad, seguridad y eficiencia.
Zeberio ve con buenos ojos el plan. Dice que es muy importante centralizar los casos y que los grupos estén bien preparados. La experiencia también es necesaria: “No es tu experiencia. El trabajo en equipo es fundamental en medicina y en estas terapias más que en ningún otro sitio. Los pacientes reciben tratamiento en el servicio de hematología, pero incluye el trabajo de profesionales de diferentes servicios, todos ellos con formación de enfermeras, intensivistas, neurólogos, infecciosos, inmunolos... Es decir, se necesita un equipo interdisciplinar, bien formado”.
Por ello, son necesarios criterios rigurosos. Según ellos, en España hay ocho centros designados para incluir terapias de células CAR-T, que no son pocos en relación a la población europea. En Euskal Herria no hay ninguna, pero Zeberio considera que no hay nada malo: “Hay que hacer las cosas bien. En la Comunidad Autónoma del País Vasco existe un plan y está decidido que en el futuro el Hospital Universitario de Donostia sea un centro de terapias CAR. Estamos preparándonos para ello”.
Mientras tanto, el seguimiento de los pacientes se realiza en el propio Hospital Universitario de Donostia-San Sebastián, pero son enviados a tratamiento a uno de estos ocho centros. Por el momento, los pacientes opcionales son aquellos que presentan tumores de la línea B con antígeno CD19, pero Zeberio espera que con el tiempo se pueda utilizar esta tecnología en otros tumores como los tumores sólidos. Cada vez se abre más la puerta a la esperanza.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian