Milers de milions per a detectar

Quan observen l'aigua, els ulls humans veuen un líquid transparent. Però si mirem amb els ulls petits dels químics tot canvia. L'aigua no és aigua, sinó una complexa mescla de milions de substàncies químiques. De la mateixa manera, el vi no és vi, un tros de formatge no és formatge i un esportista no és un esportista. Són mescles de moltes molècules.
El cas de l'aigua està indicat, per exemple, en l'etiqueta de les ampolles d'aigua. A més de l'aigua, el líquid conté ions de clorur, sulfats, nitrats, etc., i moltes altres substàncies que no s'especifiquen en l'etiqueta. I a vegades també estan representats els ions que no es consideren en l'aigua. "Aigua sense sodi". Què significa això? Que no hi ha cap ió de sodi? Normalment no, significa que el sodi, si existeix, no és detectable. En la pràctica és el mateix, la qual cosa no es pot detectar no existeix. Però potser el problema és la tècnica utilitzada per a l'anàlisi.
Els químics no detecten una sola molècula. No poden. Ni dues molècules; o deu; o mil. Han de contenir almenys mil milions de molècules per a detectar una substància. Sembla mil milions, però és una ximpleria si parlem de molècules. Hi ha moltes més molècules en gairebé qualsevol lloc.
Petits i nombrosos
Un exemple és un assaig ple d'aigua. La molècula d'aigua és petita, però molt abundant. Per a poder visualitzar les molècules d'aigua, hauríem de multiplicar la sessió per deu milions de vegades, de deu centímetres a mil quilòmetres com a mínim. Si un dels extrems d'un programa d'aquesta grandària estigués a Bilbao, per exemple, l'altre estaria a Cadis, aproximadament. Si les molècules d'aigua augmentessin en la mateixa proporció, tindrien una longitud de dos mil·límetres. Això sí, seria difícil separar les molècules perquè es mourien molt ràpid. Però serveix per a fer una idea: pensa quants molècules de dos mil·límetres entren en un assaig de mil quilòmetres de longitud.
El físic Amadeo Avogadro va trobar la quantitat: 18 mil·lilitres d'aigua a 6,023 x 10 23 molècules, gairebé un cuatrilión. Un milió té sis zeros i un bilió té dotze zeros, mentre que el número d'Avogadro, arrodonit, té vint-i-tres zeros. És un número molt gran; si s'elimina una gota d'un bilió de molècules, sembla que no es notaria el canvi (en una gota d'aigua hi ha aproximadament disset molècules de trilió).
La veritat és que la molècula de l'aigua és molt petita, les molècules orgàniques són molt més grans i no obstant això ocorre el mateix: si a una rodanxa de pernil se li lleva un bilió de molècules, l'amo no seria conscient del perdut. En aquest sentit, la detecció de mil milions de molècules sembla un miracle.
Separació de molècules
Seguint el mateix exemple d'aigua, es pot analitzar el problema del límit de detecció. Imagineu que en aquesta selva de molècules d'aigua es barregen àtoms de plom, és a dir, que l'aigua està contaminada a una concentració de 50 ppm (50 grams de plom en un milió de grams de mostra). Coneixent els pesos de l'aigua i del plom, es pot estimar que existeixen al voltant de 231.100 molècules d'aigua per cada àtom de plom. A més, les molècules d'aigua són més grans que els àtoms de plom. Per tant, la detecció de plom sembla gairebé impossible. Com es pot fer?
És clar que veure molècules no és el mètode de detecció adequat --i si existeixen tècniques de visualització-, ja que en aquest cas, a més de localitzar àtoms de plom, caldria saber quantes molècules d'aigua corresponen a cadascuna d'elles.
Però també es pot fer una altra cosa: abans de començar a detectar, dividir les molècules en grups. Depèn de la grandària, de la càrrega elèctrica, del comportament químic, etc. Una vegada dividides les molècules en grups, cada grup tindrà menys molècules que identificar i es podrà realitzar una detecció més detallada que amb la mostra inicial.
És el que es fa en els mètodes de detecció més precisos existents en l'actualitat: barrejar la mostra amb un líquid o un gas i introduir-la en un cromatògraf. El cromatògraf és una eina de separació molecular en la qual les molècules han de realitzar un recorregut ple de traves ""; unes molècules formen el recorregut ràpidament i unes altres es veuen costades. A la sortida del recorregut, les molècules apareixen dividides en grups en funció del temps que han hagut de completar el recorregut. La instal·lació d'un detector en aquesta sortida permet realitzar anàlisi a cada grup a mesura que surti.
Líquid o gas
Com més gran sigui la distribució, més precís és l'anàlisi posterior. Es tracta d'esbrinar quin cromatògraf farà la millor separació. El dubte es produeix entre el cromatògraf de gasos i líquids. Es creu que la mescla de la mostra amb el gas i la gasificació de la pròpia mostra és millor opció que la mescla amb el líquid. En definitiva, una mostra d'un determinat volum conté menys molècules si es tracta de gas.
Però, com en tot, pot haver-hi problemes. No totes les molècules són aptes per a estar en estat gasós, per exemple si són molt grans. A més, per a transformar-la en gas és necessari escalfar la mostra i no totes les molècules superen aquest procés: es degraden molt abans d'evaporar-se. En aquest sentit, el líquid és més útil. Una dissolució és senzilla en seleccionar el dissolvent apropiat.
Per tant, depenent de la substància a detectar, la distribució es realitza mitjançant un cromatògraf o un altre. El mateix ocorre amb els detectors. Triar la més adequada en funció de la substància a detectar. Alguns detectors són molt especialitzats, serveixen per a detectar una determinada substància, però amb uns altres no són precisos o no serveixen.
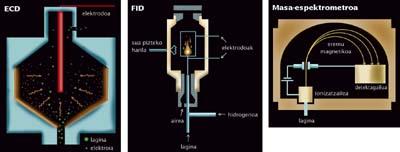
En el rànquing de detecció de les menors quantitats de substàncies, en l'actualitat cal citar tres: FID, ECD i espectròmetre de masses. Darrere d'aquests noms es troben els detectors més precisos del món, els millors detectors que existeixen per a buscar traces moleculars. Els tres s'utilitzen conjuntament amb cromatògrafs de gasos. Però no sempre. La parella formada per l'espectròmetre de masses i la cromatografia de líquids també està aconseguint un gran èxit en els últims temps.

Inexacta
Quatre mètodes ofereixen resultats sorprenents. Per diferents motius és difícil comparar els quatre, però si haguéssim de triar el més cridaner seria el cromatògraf de gasos/parell ECD. El detector ECD és un detector extremadament precís: pot detectar només alguns piccogramas d'una substància (un pícogramo és el d'un bilió d'un gram). Si, per exemple, la utilitzéssim per a detectar el clorur de vinil, bastarien al voltant de mil milions de molècules per a detectar ECD.
Les parelles que formen els FID i l'espectròmetre de masses amb cromatògraf de gasos són menys precises. Els nanogramos "només" arriben a detectar-se, per exemple, necessiten un bilió de molècules per a trobar les petjades del clorur de vinil.
I quin èxit té el cromatògraf de líquids? Normalment, en lloc de donar el pes que el cromatògraf pot detectar, els venedors donen concentració. Les dades més optimistes són sorprenents: alguns equips són capaços de trobar concentracions de 500 granulomes per litre, és a dir, mantenint l'exemple del clorur de vinil, detectarien deu milions de molècules en un litre de dissolució.
Versió d'usuari

Els números han de prendre's amb molta cura. Aquestes dades són dades dels venedors que indiquen els límits de detecció del mètode. Però la realitat sempre és més complexa.
Cada mètode proporciona límits de detecció en determinades condicions. I mitjançant el mesurament de determinades molècules. El detector ECD és molt bo amb substàncies halogenades (per això el clorur de vinil és un bon exemple pel seu contingut en clor). Per part seva, el FID detecta molècules carbonadas (moltes són però moltes no contenen carboni).
No obstant això, també es pot dir el contrari. Les tècniques actuals satisfan la necessitat social de precisió en la detecció de substàncies.


Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian











