La teràpia gènica des de l'esperança a la realitat

La teràpia gènica pretén resoldre l'error de manera radical, ja que utilitza seqüencies ADN per a transformar cèl·lules malaltes i aconseguir un efecte terapèutic. D'aquesta forma s'aconsegueix sintetitzar la molècula que les cèl·lules defectuoses fabricaven.
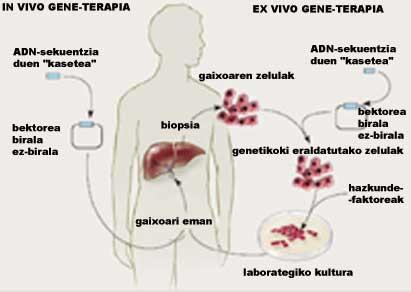
El canvi genètic pot realitzar-se de dues formes. Ex viu és una teràpia que consisteix a extreure cèl·lules al pacient, modificar-les genèticament en el laboratori i aplicar-les de nou al pacient. En la manera in vivo les cèl·lules es transformen sense ser extretes. La figura 1 mostra les principals diferències entre les dues teràpies. Recentment s'ha desenvolupat una tercera forma en la qual les cèl·lules universals (que no són del pacient) són modificades genèticament i aplicades al pacient. En aquest cas, les cèl·lules s'insereixen sol o en càpsules.
Introducció a la teràpia gènica
La primera sessió clínica de teràpia gènica la va realitzar el grup de Rosenberg en 1990. Els pacients amb càncer cutani molt desenvolupat van ser tractats amb limfòcits genèticament modificats. Des de llavors s'han posat en marxa més de 500 sessions clíniques de teràpia gènica a tot el món. Al principi es tractava de resoldre les alteracions produïdes per un únic gen, substituint el gen defectuós per còpies sense defectes. Per exemple, fibrosi quística, distròfia muscular de Duchenne o hipercolesterolemia familiar. Posteriorment, les cèl·lules van ser modificades genèticament i tractades malalties complexes d'origen genètic desconegut. Per a això s'han utilitzat estratègies citotòxiques (causants de la mort cel·lular) i citostàtiques (que impedeixen la proliferació cel·lular) com el càncer o alguns tipus de cardiopaties.

En resum, al llarg d'aquests 10 anys les aplicacions de la teràpia gènica han crescut de manera constant, al mateix temps que s'ha fet un gran esforç en la cerca de noves vies d'aplicació. L'objectiu és que aquestes vies siguin més eficients i menys tòxiques.
Requisits essencials de la teràpia gènica
Què cal tenir en compte a l'hora de definir la teràpia gènica? En primer lloc, tres coses: amb quines cèl·lules o teixits es treballarà, quina estratègia s'utilitzarà (ex viu, in vivo o cèl·lules universals) i, per descomptat, quin producte (insulina, leptina, factors de coagulació...) vol que les cèl·lules les produeixin. La seqüencia ADN. Una vegada definida i adquirida la seqüència ADN es guarda en un ‘casset’. El ‘casset’ és una seqüència sintètica en la qual es troben els elements que regulen la representació de l'ADN.
A continuació es detalla com es transportarà la seqüencia ADN fins a les cèl·lules defectuoses del malalt. Generalment s'utilitzen vectors. Els vectors són transportadors de gens la missió dels quals és la transferència del gen terapèutic a la cèl·lula defectuosa i assegurar la correcta expressió del gen. Existeixen molts vectors, però es classifiquen en virals i no virals (veure figura 2).
Normalment els vectors no virals mantenen el ‘casset’ dins o en superfície. Les més comunes són les formades per lípids catiònics (lipoplexos) i polímers catiònics (poliplexos). La major part d'elles produeixen una baixa resposta immulógica que impedeix la inflamació del pacient. No obstant això, els vectors no virals tenen poca efectivitat en la transferència del gen i, a més, només l'expressen a curt termini.
Els vectors virals, per part seva, es basen en la capacitat dels virus d'arribar a les cèl·lules i expressar els gens de manera significativa. Els avanços científics han aconseguit millorar substancialment l'expressió i seguretat dels vectors virals, però la toxicitat continua sent el principal obstacle a superar per aquests vectors.
Finalment, s'ha de definir com s'inserirà el vector en els òrgans o teixits del pacient, és a dir, si es realitzarà mitjançant xeringa, catèter, ... o d'una altra manera.
Situació actual
Actualment la teràpia gènica s'aplica en moltes malalties. S'han realitzat sessions clíniques en diferents laboratoris i s'ha provat l'eficàcia i toxicitat de la teràpia gènica en humans. A la vista dels avanços de l'última dècada es pot afirmar que la teràpia gènica té un gran futur, sempre que es respectin les malalties i els pacients. La Fundació Marcelino Botin va organitzar un seminari sobre el present i futur de la teràpia gènica en la Universitat Internacional Menéndez Pelayo, en el qual es van mostrar alguns exemples dels avanços esmentats. Diabetis, hemofília, malalties cutànies, càncer, alteracions de les cèl·lules sanguínies, etc. es van presentar estratègies de tractament mitjançant teràpia gènica.
Els investigadors reunits a Santander van determinar les condicions per a poder aplicar la tecnologia de teràpia gènica. En primer lloc, la transferència adequada de la seqüència ADN a les cèl·lules malaltes és imprescindible, així com la indicació del producte a llarg termini. Al mateix temps, s'ha de reduir al màxim la toxicitat d'aquests sistemes per a evitar efectes secundaris adversos. Si es vol treballar amb cèl·lules que s'implantaran en animals o persones, és necessari trobar bons sistemes de cultiu en el laboratori i procediments de trasplantament adequats i assegurances.
Grups del projecte de Biologia Molecular, Cel·lular i Teràpia Gènica de Ciemat, Jose L. Sota la direcció de Jorcano, utilitza la teràpia gènica per a regenerar l'epidermis i presenta els seus resultats a Santander. Es pretén aconseguir una pell artificial útil per a pacients amb cremades, psoriasis o úlceres cròniques. Per a això s'ha comptat amb l'estratègia in vivo i han creat una pell que treballa com bioreactor a través de l'alliberament de substàncies beneficioses.
L'hemofília també desperta gran interès entre els investigadors. Gonzalo Hortelano, professor de la Universitat Canadenca de McMaster, utilitza la teràpia gènica per a combatre l'hemofília. Els pacients amb hemofília flueixen pocs IX factors sanguinis. El professor Hortelano ha modificat genèticament algunes cèl·lules perquè flueixin aquest factor i les ha introduït en microcápsulas. De moment només els ha provat amb ratolins de laboratori, però espera iniciar sessions clíniques a mitjà termini. Katherine A. El grup d'High utilitza vectors virals per al tractament de l'hemofília. Recentment s'han iniciat sessions clíniques per a analitzar l'eficàcia i toxicitat d'aquesta estratègia en els éssers humans. Segons el Dr. High, els bons resultats preliminars permeten que els primers productes de teràpia gènica estiguin preparats en 2004.
Sens dubte, el càncer és la malaltia que més sessions de teràpia gènica ha impulsat. L'any 2000 es van aprovar als Estats Units més de 300 protocols. Però és tan gran com l'interès que desperta la complexitat del càncer. En el procés de creació del tumor intervenen molts gens i cal tenir en compte molts factors.
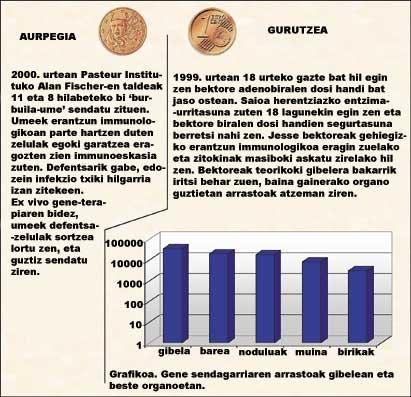
En general, els resultats de la teràpia gènica són positius, però no tan espectaculars com es pensava al principi. Per tant, procedeix analitzar les dues cares de la moneda (veure figura 3). El major èxit el va obtenir l'Institut Pasteur l'any passat, quan va curar ‘nens de bombolles’ mitjançant un programa ex viu. Va ser la primera vegada que es curava totalment una patologia mitjançant teràpia gènica. Desgraciadament, en la creu de la moneda es troba la mort del jove Jesse. Va morir en 1999 en un intent clínic de prova d'adenobirus.
Obstacles i futur

Abans d'arribar als hospitals, la teràpia gènica ha de superar una sèrie d'obstacles. La majoria dels investigadors consideren que les majors dificultats són les tecnològiques. En aquest sentit, és evident la necessitat d'optimitzar els tres components bàsics de la teràpia gènica: Seqüència d'ADN, vectors i via d'administració. Els genetistes han descobert les bases genètiques de malalties causades per un únic gen o per un grup de gens. Els vectors, tant virals com no virals, són cada vegada més eficients i mostren seguretat a llarg termini. És possible que en aquests anys s'hagi produït un menor desenvolupament de la via de tractament degut a la gran quantitat de factors tecnològics i biofarmacéuticos a tenir en compte per a aconseguir una correcta obtenció.
La transformació dels principis actius en dosis segures i efectives ha estat sempre un dels objectius fonamentals de la recerca farmacèutica. Sembla, per tant, raonable pensar que augmentaran els esforços que les institucions públiques i les empreses privades realitzen en aquest camp. De fet, l'expectativa d'ús de la teràpia gènica depèn en gran manera de la correcta administració de les dosis. Per a això serà necessari que investigadors de diferents àrees coordinin els seus esforços.
Com s'ha vist, la teràpia gènica té més requeriments que altres teràpies, i les responsabilitats ètiques també són majors. La seguretat dels pacients que participen en les sessions clíniques no pot veure's en cap cas compromesa pels patrocinadors o per les expectatives creades. Els investigadors han de deixar clar que la teràpia gènica està en desenvolupament i que no curarà moltes malalties abans de la dècada vinent. A més, és fonamental que els pacients, les seves famílies i les organitzacions reguladores coneguin amb precisió els beneficis i riscos potencials de la teràpia gènica experimental.
No obstant això, aquest enfocament realista no ha d'afeblir la il·lusió per la teràpia gènica. La teràpia gènica i altres alternatives prometedores com les cèl·lules mare es troben en una fase inicial. Al contrari del que es va fer amb la teràpia amb medicaments, els avanços s'estan realitzant respectant el punt de vista científic i no provant els medicaments amb els pacients i veient el seu efecte. És sens dubte la millor garantia d'un futur pròsper.
Naturalesa del vector | Avantatges | Molèsties |
BIRALA Retrovirus | BIRALA s'integra en Genoma Perdura a llarg termini | VIRAL Només afecta a cèl·lules en divisió |
Adenobirus BIRALA (AB) | VIRAL Comú en humans Afecta a cèl·lules que no es divideixen | VIRALA Baixa resposta immunològica |
BIRALA Lentivirus Units | VIRALA Afecta a les cèl·lules que no es divideixen Resultats esperançadors | VIRAL Baixa capacitat de transport d'ADN Toxicitat? ?? |
NO VIRAL Lipoplexos Poliplexos | NO VIRAL Provoquen una resposta immunològica baixa o nul·la | NO-VIRAL Indiquen el gen amb poc temps |
Opinions capdavanteres
Per què van optar per investigar en teràpia gènica?
J.L.J. : D'una banda, perquè es tracta d'una àrea de recerca prometedora i per tant, de recerca. D'altra banda, a l'ésser un laboratori que realitzem la recerca bàsica de la pell, ens resultava fàcil realitzar la part terapèutica de la recerca i decidim intentar-lo.

S.W. : Perquè la teràpia gènica és un tema científic apassionant que acaba de néixer i estem en etapes preliminars. Les bases científiques i clíniques de la teràpia gènica són fecundantes i la utilització del nostre material genètic per a tractar malalties fa una estratègia molt poderosa. Per aquestes raons estem desenvolupant la tecnologia d'alliberament de gens en cèl·lules i teixits adequats.
G.H. : Teràpia gènica XXI. Crec que exercirà un paper important en la medicina del segle XX. En aquests moments és un tema científic incipient i em sembla molt atractiu participar en el desenvolupament d'aquest camp de recerca en la mesura que sigui possible.
Què ofereix la teràpia gènica sense altres tractaments?
J.L.J. : La teràpia gènica ofereix una alternativa a les malalties. Aborda la malaltia des d'un punt de vista científic i no com s'ha fet amb els medicaments ortodoxos, provant i observant els resultats. La teràpia gènica es basa en un coneixement científic més profund, en el coneixement dels gens relacionats amb les malalties i pretén utilitzar-los per a curar-los. Però ha estat més complicat del que inicialment es pensava.
S.W. : La teràpia gènica té un avantatge important que la diferència d'altres teràpies. Altres mètodes terapèutics, com la cirurgia, radiacions, medicaments, etc. estan dissenyats per a extirpar una malaltia o una funció corporal. La teràpia gènica, en canvi, subministra el cos, li dóna una substància que no tenia. En el cas d'una malaltia genètica, l'aplicació d'un gen sense defectes permet curar la malaltia. Aquest tipus de tractaments també poden aplicar-se a altres patologies com el càncer o la sida.
G.H. : És cert que la farmacologia tradicional porta dècades preparant fàrmacs eficaços per a modificar determinades funcions fisiològiques. Però la teràpia gènica ofereix la possibilitat d'administrar medicaments de manera contínua i constant. Els medicaments tradicionals no poden proporcionar aquesta estabilitat crítica en molts processos fisiològics. A més, en alguns casos només és teraupeutico quan el producte està dins de les cèl·lules, no en sang. Llavors, els medicaments no sempre són efectius. D'altra banda, l'ús de material genètic obre les portes a noves alternatives, com la possibilitat de generar noves respostes immunològiques en el cos. Finalment, i especialment en el cas de les malalties cròniques, la teràpia gènica pot reduir considerablement el cost dels tractaments. En el cas de l'hemofília, per exemple, s'espera que un únic tractament de teràpia gènica substitueixi a les injeccions actuals. Ara el pacient ha d'injectar-se diverses vegades per setmana al llarg de tota la vida.

Quins són els principals obstacles que ha de superar la teràpia gènica? Tecnològiques? Biològics? Ètiques?
J.L.J. : Jo no crec que hi hagi obstacles ètics. Cal tenir en compte l'ètica, però canvia de persona a persona. Per exemple, l'ètica del pacient és diferent de la de l'investigador, i la de l'investigador i la del periodista. Amb això no vull menysprear a ningú, sinó dir que l'ètica és important i a tenir en compte en la nostra societat. Però avui dia els nostres problemes són tecnològics, no ètics. Els vectors per a la introducció de gens terapèutics en les cèl·lules no són tan perfectes com volíem i les malalties són molt més complexes del que pensem. Sabem massa poc i de moment només podem curar malalties causades per un únic gen defectuós. Però en la majoria de les malalties intervenen molts gens, on predomina el desconeixement.
S.W. : Des del punt de vista tecnològic, el principal inconvenient és l'especificitat, és a dir, com alliberar selectivament el gen en la cèl·lula desitjada. El control de l'activitat del gen també és molt important. Volem que el gen s'expressi de manera que es produeixi un efecte terapèutic i evitar els efectes nocius. D'altra banda, és important investigar quines malalties es poden curar mitjançant teràpia gènica i quins no. Des del punt de vista ètic, la comunitat científica té molt clar que l'utilitzarà per a curar la teràpia gènica, no per a millorar a l'home. La teràpia gènica és una estratègia per a tractar malalties, no una tècnica per a estimular les habilitats d'una persona.
G.H. : Crec que les majors dificultats tècniques estan relacionades amb els vectors. El vector opcional ha de garantir la seguretat del pacient i tenir una eficàcia terapèutica en aquest ordre, a més de permetre el seu reemisión. D'altra banda, considero que la gran variabilitat d'una persona a una altra és un factor a tenir en compte. Avançament que l'èxit de la teràpia gènica es limitarà al principi a unes poques malalties. Posteriorment s'anirà estenent progressivament.
Les grans expectatives generades per la teràpia gènica han beneficiat o perjudicat el vostre treball?

J.L.J. : A mi no m'han influït res, però és cert que ocorre moltes vegades i, per exemple, el que viuen en el genoma. En aquests moments la biologia ha recollit coneixements suficients per a passar de ser ciència bàsica a ciència aplicada, és a dir, abans ens acostàvem a estudiar a biologia, però ara volem treure-li partit a ella. La teràpia gènica i la genòmica han nascut d'aquest canvi i les percebem com una aplicació. En el cas de la teràpia gènica la idea és bastant senzilla. Pretenem conèixer les bases moleculars de les malalties i identificar els gens defectuosos per a la seva posterior curació.
Tenim mitjans i capacitat per a fer-ho tot en el laboratori, però tot ha estat més complicat del que pensem al principi. I per tant, hem passat del cim de l'optimisme a la pressió de les expectatives. Però la realitat està a mig camí. La teràpia gènica ha donat bons resultats en els últims anys i gràcies a això sabem que els objectius no són impossibles, però tampoc fàcils. La qüestió és que la biologia és ciència aplicada. Hi ha gent que ven idees i s'està enriquint en 24 hores i d'aquí sorgeixen les expectatives.
S.W. : Crec que la pessimisme va aparèixer sobretot fa dos anys, quan va morir un pacient en una sessió clínica. Va ser llavors quan va sorgir la mala imatge de la perillosa teràpia gènica. En conseqüència, investigadors i responsables de la regulació de les sessions clíniques van tornar enrere i van revisar exhaustivament tots els protocols. L'incident ha fet que els requisits per a iniciar una sessió clínica siguin majors i el control sigui molt més estricte. La mort de fa dos anys va ser tràgica, però vam aprendre molt.
G.H. : Jo crec que li ha fet mal. Han despertat falses expectatives entre malalts i familiars i el mateix sentiment s'ha estès a tota la societat. En aquest ambient de calidesa s'han iniciat nombroses sessions clíniques, encara que algunes amb escassa base científica. Com a conseqüència, moltes sessions han fallat. A la vista d'aquests resultats descoratjadors, s'ha posat més èmfasi a augmentar els coneixements bàsics de teràpia gènica i s'han obtingut els primers resultats esperançadors.
Gorka Orive Rierol
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian