Microbiota i malaltia metabòlica
2024/03/01 Azkarate Irigoras, June - Biokimika eta Biologia Molekularra sailaEHU | Manzanares Gómez, Aitor - Biokimika eta Biologia Molekularra sailaEHU | Benito Vicente, Asier - Biokimika eta Biologia Molekularra sailaEHU Iturria: Elhuyar aldizkaria
La relació microbi-metabolisme ha obert noves portes en el món de la recerca en les últimes dècades. El nostre organisme està format per microorganismes la composició equilibrada dels quals exerceix un paper fonamental en la salut. L'obesitat, la diabetis o la síndrome metabòlica són malalties que poden ser causades per desequilibris en aquesta composició.
En 1914, el filòsof Ortega y Gasset va dir la famosa frase “Jo soc jo i les meves circumstàncies”. En aquest cas, ens ve millor la frase “Jo soc jo i la meva microbiota”.
El microbiota està format per tots els microorganismes que viuen en el nostre organisme. Està format principalment per bacteris, però també apareixen fongs, llevats i virus, entre altres [1]. Com els virus? Tranquil, la relació entre el nostre organisme i aquests microorganismes és generalment simbiòtica, és a dir, beneficiosa per a totes dues parts. De fet, mantenen l'estat fisiològic normal del cos en un equilibri dinàmic [2] i participen en la immunitat [3].
El microbiota es troba en el nostre cos en qualsevol lloc en contacte amb el mig extern: intestí (famosa flora intestinal), boca, pell i vagina [1]. En total, conté 38 bilions de microorganismes, més de 30 bilions de cèl·lules humanes corporals [4]. Dit d'una altra manera, les cèl·lules microbianes són més abundants en el nostre cos que les cèl·lules humanes.
El microbiota intestinal o flora intestinal és la microbiota més important i variable. Es caracteritza per la seva complexitat, dinamisme i heterogeneïtat [2].
Complex per la gran varietat de microorganismes. No obstant això, com ocorre amb els cognoms, hi ha grups de bacteris molt nombrosos: Firmicutes, Bacteroidetes, Actinomycetes, i Proteus [2]. És dinàmic perquè pot variar segons la dieta o l'estil de vida. Finalment, és heterogeni perquè la composició de la flora intestinal varia d'una zona a una altra.
Com ja s'ha esmentat, dins del nostre cos es troba un apassionat món microbià, petits organismes que juguen un paper fonamental en la nostra salut. Curiosament, aquesta comunitat microbiana comença a formar-se abans de néixer, ja que la seva mare la transmet al fetus [5].
No obstant això, continua el seu desenvolupament postnatal, en el qual influeix el mètode del part, la dieta (lactància materna o de fórmula), la higiene i l'ús d'antibiòtics. Cal destacar que els tres primers anys de vida són indispensables per a la formació d'un microbiota estable similar a un adult, una comunitat microbiana que, posteriorment, influeix de manera significativa en el nostre sistema immunològic i neurològic [5].
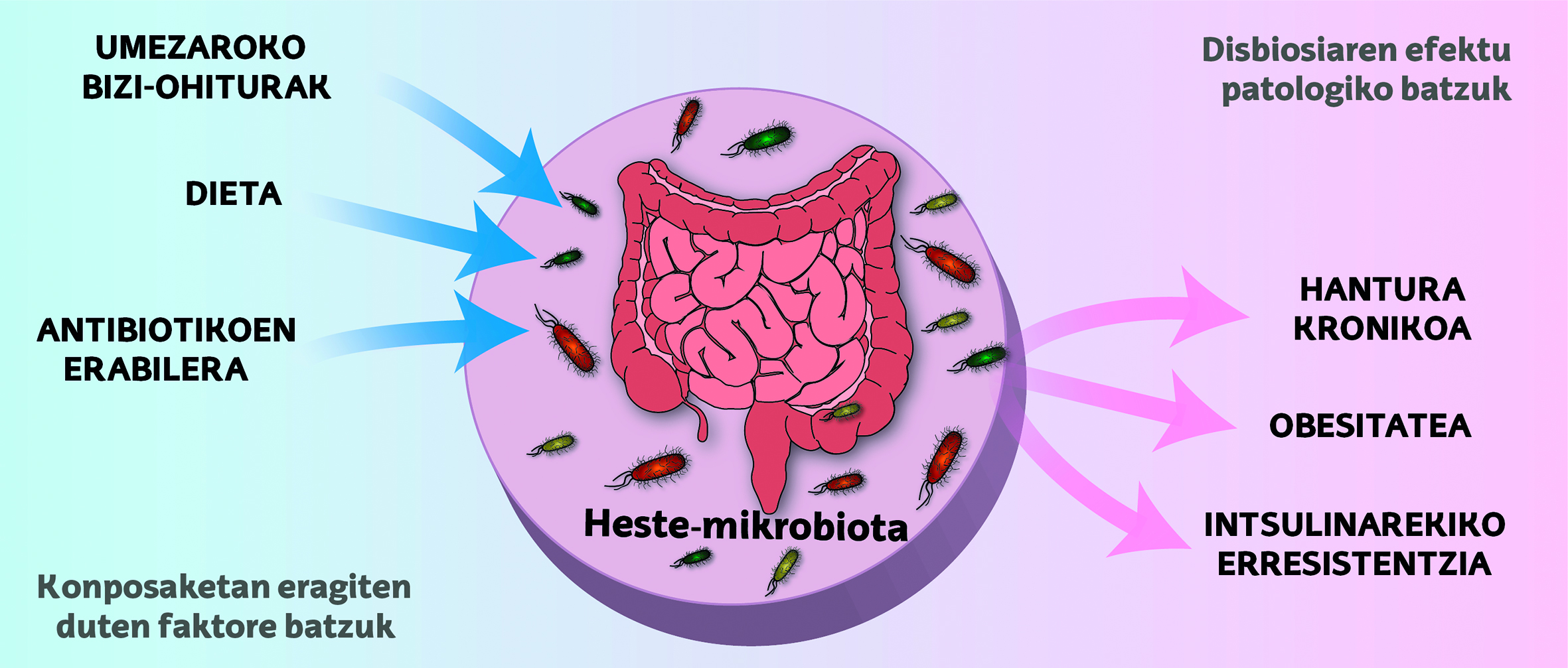
No obstant això, al llarg de la vida, l'ecosistema intestinal pot sofrir alteracions que afecten el delicat equilibri entre els microbis i el nostre cos, situació que es coneix com disbiosis. Aquestes alteracions poden ocasionar problemes com a inflamació, trastorns metabòlics o resistència a la insulina, la qual cosa augmenta el risc de patir malalties metabòliques (Figura 1) [5].
La comunitat de microorganismes que habita en el nostre intestí ha tingut un interès científic creixent en les últimes dècades. A mesura que s'aprofundeix en la comprensió d'aquesta xarxa biològica, s'han trobat connexions clarificadores entre la composició microbiana i diferents estats de salut, incloent-hi diabetis, obesitat i síndrome metabòlica.
Obesitat
Tots sabem el que és l'obesitat, però com l'Organització Mundial de la Salut la defineix? L'obesitat és una acumulació excessiva de greix, perillosa per a la salut [6].
I d'on surt aquest greix? Perquè, en definitiva, és el resultat d'un balanç energètic positiu [7]. És a dir, es produeix quan les calories que prenem de la dieta superen les que el nostre organisme necessita per a exercir les seves funcions.
Però per què no engrossir al meu amic si no fa esport i menja un munt? L'obesitat, com la majoria de les malalties, també depèn dels gens [8]. Però últimament s'ha vist que el microbi també influeix.
En un estudi es van comparar els microbis de ratolins obesos i ratolins prims [9]. Els polisacàrids (molècules de sucre grans i complexes) que no podem digerir i absorbir els mamífers poden digerir els microbis dels ratolins obesos per tenir unes artazas per a això. Gràcies a aquestes tisores anomenades enzims, els polisacàrids es tallen i es transformen en sucres simples que poden absorbir.
Per tant, en resum, els ratolins obesos aprofiten millor les calories ingerides gràcies a la seva microbiota. De fet, la femta de ratolins obesos tenen menys calories. Per això, encara que els ratolins obesos i els ratolins prims s'alimenten per igual, el balanç energètic dels ratolins obesos serà més positiu i acumularan greix. És més, trasplantant el microbiota dels ratolins obesos en ratolins prims, els ratolins prims comencen a acumular greix.
Tot això, evidentment, es pot extrapolar als éssers humans. I sí, encara que sembli avorrit, la manipulació microbiana pot convertir-se en una important estratègia terapèutica per a regular el balanç energètic de les persones obeses [7].
Diabetis i síndrome metabòlica
Ja hem vist l'obesitat, però com es pot definir la diabetis i la síndrome metabòlica? La síndrome metabòlica és un conjunt d'anomalies metabòliques que fan referència a la coexistència de diversos factors de risc per al desenvolupament de la malaltia cardiovascular. Entre aquestes anomalies metabòliques es troba la resistència a la insulina, entre altres [10]. La diabetis és una malaltia crònica que es produeix quan l'àrea no segrega suficient insulina o el cos no utilitza eficaçment la insulina produïda [11]. Però, de què parlem quan parlem d'insulina? La insulina és una hormona que regula la concentració de glucosa en sang, la glucèmia. Quan la concentració de glucosa en sang és molt alta, s'aconsegueix alliberar l'hormona insulina i disminuir la concentració, mantenint una regulació adequada [12].
Clar, no? Així doncs, per a continuar avançant en aquesta història, ha arribat l'hora de presentar als participants TLR!
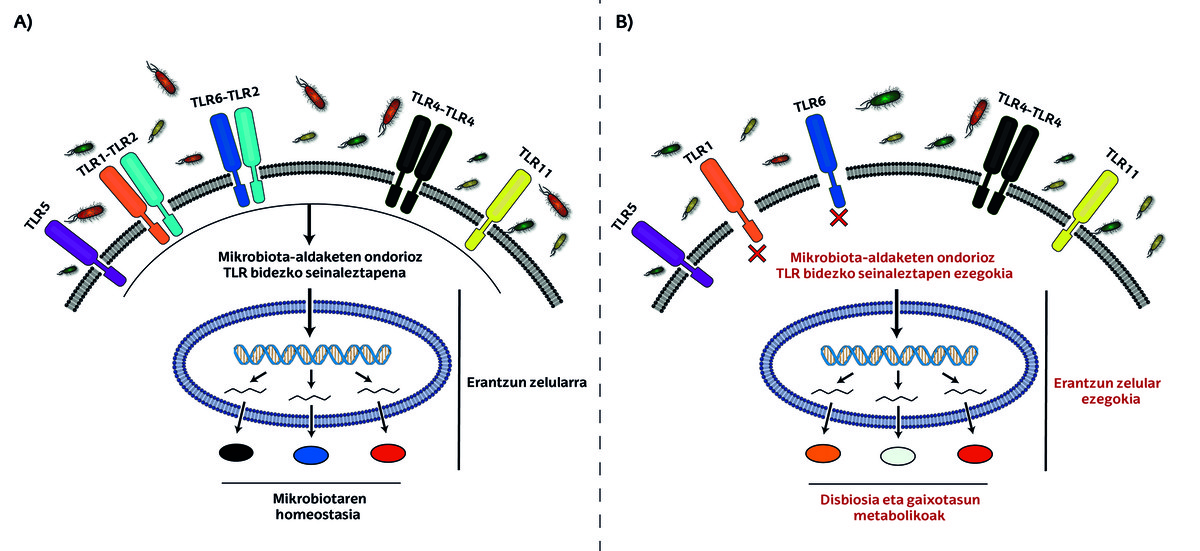
Els TLR o Receptors Tipus Toll són antenes microscòpiques que detecten senyals en el nostre cos. Aquests receptors apareixen en les cèl·lules de l'epiteli intestinal i regulen la colonització bacteriana, és a dir, s'encarreguen de mantenir les quantitats dels diferents bacteris a un nivell adequat [13].
Encara que existeixen molts subgrups dins de la família TLR, el TLR2 és especialment important en la diabetis. S'observa que en la flora intestinal de ratolins sense receptor TLR2 hi ha menys bacteris del gènere Bifidobacterium. Aquests bifidobacterium actuen com a pegats en l'intestí i la seva manca provoca un augment de la permeabilitat intestinal. Això provocarà que les toxines bacterianes travessin l'epiteli intestinal i entrin en circulació, provocant una inflamació que augmentarà el risc de patir diabetis mellitus. Aquest mecanisme ens permet dues possibilitats de tractament. D'una banda, es poden utilitzar antibiòtics que ataquen bacteris d'altres gèneres per a afavorir la proliferació de bacteris del gènere Bifidobacterium. D'altra banda, el microbiota de ratolins sans es pot trasplantar en la flora intestinal de ratolins sense TLR2 [7].
Així mateix, el desequilibri d'alguns bacteris intestinals pot causar problemes directament relacionats amb la resistència a la insulina i, per tant, amb la diabetis. Com ja s'ha comentat, la insulina regula la concentració de glucosa en sang. Si es desenvolupa la resistència a la insulina, les cèl·lules del cos no podran respondre adequadament a la insulina. En principi, el cos pot mantenir els nivells de sucre en la sang dins del nivell normal, augmentant la producció d'insulina. No obstant això, a mesura que la resistència a la insulina empitjora i el pàncrees no pot continuar generant insulina suficient per a superar-la, els nivells de glucosa en sang augmenten, la qual cosa comporta diabetis tipus II. La diabetis tipus II pot entendre's, per tant, com una hiperglucemia causada per la resistència a la insulina [14].
Confirmant l'exposat, s'han trobat relacions entre la composició microbiana i la resistència a la insulina en persones amb diabetis tipus II [7]. Així les coses, el tema de la diabetis tipus II ha quedat clar, però què ocorre amb la diabetis tipus I? El microbiota també es pot associar a la diabetis tipus I, una malaltia autoimmune que es dona en les etapes precoces de la vida. Una malaltia autoimmune és una alteració produïda pel propi sistema immunitari que afecta les cèl·lules del propi organisme. En aquest cas, la diabetis tipus I destrueix selectivament algunes cèl·lules de l'àrea i causa dèficit d'insulina [15]. En estudis amb ratolins i ratolins s'ha observat que alguns bacteris intestinals afecten la incidència d'aquesta malaltia i que el desequilibri dels TLR i la composició modificada del microbiota poden provocar diabetis tipus I [7].
Finalment, i seguint amb els ratolins, en els estudis realitzats amb aquests animals, es va observar que els criats en ambient lliure de gèrmens (amb tots els receptors TLR a un nivell adequat) estaven protegits de la resistència a la insulina, l'obesitat i altres malalties, a pesar que la dieta proporcionada era rica en greixos. Per contra, la colonització d'aquests ratolins protegits amb microbiosis intestinal de ratolins amb deficiència de receptor concret TLR5 va portar a un ràpid desenvolupament de la síndrome metabòlica. L'estudi va revelar la relació de la síndrome metabòlica amb el microbi. Com si fos poc, en els éssers humans també s'han identificat comunitats específiques de bacteris intestinals relacionats amb la síndrome metabòlica [7].
Encara queda molt per investigar sobre el microbiota. Els avanços tècnics permeten comprendre cada vegada millor els mecanismes sota l'obesitat, la diabetis, la síndrome metabòlica i altres malalties, així com les seves interrelacions. D'aquesta manera, s'obre la porta a noves possibilitats de prevenció i tractament en el futur, al mateix temps que s'espera poder alleujar la càrrega d'aquestes malalties en els sistemes sanitaris.
Bibliografia
[1] Hou, Kaijian, Zhuo Xun Wu, Xuan Yu Chen, Jing Quan Wang, Dongya Zhang, Chuanxing Xiao, Donen Zhu, Jagadish B. Koya, Liuya Wei, Jilin Li, and Zhe Sheng Chen. 2022. “Microbiota in Health and Diseases.” Signal Transduction and Target Therapy 7(1).
[2] Chen, Yinwei, Jinghua Zhou, and Li Wang. 2021. “Role and Mechanism of Gut Microbiota in Human Disease.” Frontiers in Cellular and Infection Microbiology 11.
[3] Belkaid, Yasmine, and Oliver J. Harrison. 2017. “Homeostatic Inmunity and the Microbiota.” Inmunity 46(4):562–76.
[4] Sender, Ron, Shai Fuchs, and Ron Milo. 2016. “Revised Estimates for the Number of Human and Bacteri Cells in the Bodi.” PLoS Biology 14(8). just: 10.1371/journal.pbio.1002533.
[5] Boulangé, Claire L., Ana Luisa Neves, Julien Chilloux, Jeremy K. Nicholson, and Marc Emmanuel Dumas. 2016. “Impact of the Gut Microbiota on Inflammation, Obesity, and Metabolic Disease.” Genome Medicine 8(1).
[6] https://www.who.int/health-topics/obesity#tab=tab_1
[7] Hemarajata, Peera, James Versalovic, and Estel Dra Lau. 2013. “Traduccions Polítiques del Clinical Chemistry La Microbiota Intestinal Humana i El Metabolisme Corporal: Assumpció de L'Obesitat i La Diabetis`Sridevi Diabetis`Sridevi.” Acta Bioquím Clín Latam 47(2):617–45.
[8] Singh, Esberlen Kumar, Permendra Kumar, and Kulandaivelu Mahalingam. 2017. “Molecular Genetics of Human Obesity: A Comprehensive Review.” Comptes Rendus - Biologies 340(2):87–108.
[9] Turnbaugh, Peter J., Ruth E. Llei, Michael A. Mahowald, Vincent Magrini, Elaine R. Mardis, and Jeffrey I. Gordon. 2006. “An Obesity-Associated Gut Microbiome with Increased Capacity for Energy Harvest.” Nature 444(7122):1027–31. just: 10.1038/nature05414.
[10] Huang, Paul L. 2009. “A Comprehensive Definition for Metabolic Syndrome.” Disease Models & Mechanisms 2(5–6):231–37. just: 10.1242/dmm.001180.
[11] Darenskaya, M. A. L. I. Kolesnikova, and S. I. Colesnikov. 2021. “Oxidative Stress: Pathogenetic Role in Diabetis Mellitus and Its Complications and Therapeutic Approaches to Correction.” Bulletin of Experimental Biology and Medicine 171(2):179–89. just: 10.1007/s10517-021-05191-7.
[12] Andrali, Sreenath S., Megan L. Sampley, Nathan L. Vanderford, and Sabire Özcan. 2008. “Glucose Regulation of Insulin Gene Expression in Pancreatic β-Cells.” Biochemical Journal 415(1):1–10. just: 10.1042/BJ20081029.
[13] Yiu, Jensen H. C. Bernhard Dorweiler, and Connie W. Woo. 2017. “Interaction between Gut Microbiota and Toll-like Receptor: From Inmunity to Metabolism.” Journal of Molecular Medicine 95(1):13–20. just: 10.1007/s00109-016-1474-4.
[14] Ta, Azez. 2020. “Hypomagnesemia and Insulin Resistance: Gaining Better Understanding of the Pathophysiology of Type 2 Diabetis.” Diabetis. Insights Biomed 5(4):12. ajust: 10.36648/2572-5610.4.4.76.
[15] Chellappan, Dinesh Kumar, Nandhini S. Sivam, Kai Xiang Teoh, Wai Pa Leong, Tai Zhen Vaig ser, Kien Chooi, Nico Khoo, Fam Jia Yi, Jestin Chellian, Lim Lay Cheng, Rajiv Dahiya, Gaurav Guamvi, Sbramvi, Singnmi, Sfray, Singnmi, Smi, Sfray, Singnmi, Sfray, SSingnmi, Smi. 2018. “Gene Therapy and Type 1 Diabetis Mellitus.” Biomedicine & Pharmacotherapy 108:1188–1200. just: 10.1016/j.biopha.2018.09.138.

Gai honi buruzko eduki gehiago
Elhuyarrek garatutako teknologia



_display_home.jpg)

