Terras raras
Denomínanse terras raras aos 17 metais situados entre elementos químicos de número atómico 21 e 71, así como aos compostos que os producen.
Estes dezasete elementos son: Tres elementos do grupo III b [Escandio (Sc), Itrio (E) e Lantano (A)] e a primeira das dúas series, comunmente denominadas lantánido, que se escriben fóra da táboa periódica, composta por 14 elementos. O nome de lantánido débese á súa descendencia. A serie de lantánidos componse de: Cerio (Ce), Praseodimio (Pr), Neodimio (Nd), Prometio (Pm), Samario (Sm), Europio (Eu), Gadolinio (Gd), Terbio (Tb), Disprosión (Dy), Holmio (Ho), Blutitorio (Blu).
Historia
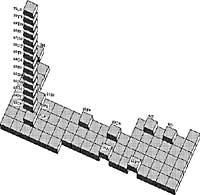
Nome de terra rara, XVIII. Desde o século XX, data na que se realizaron os primeiros descubrimentos sobre estes metais. A proporción destes metais era mínima naqueles minerais dos estudos iniciais. Ante esta escaseza, estes investigadores creron que eran moi raros na superficie terrestre. Posteriormente púidose comprobar que estaban equivocados. O cerio, o lantano e o neodimio son máis abundantes na superficie terrestre que o chumbo. O itrio é máis común que o estaño e a cortiza terrestre é tan rica en tulios como en iodos.
A historia científica destes elementos é moi turbulenta. A investigación de moitos anos de dureza, mestura e paso a paso tras o coñecemento acumulado até a actualidade. Entre o primeiro descubrimento dun elemento desta familia e o último en illar pasaron 144 anos. Tardou medio século en descubrir que o didimio era una mestura de neodimio e praseodimio.
A longa historia da investigación sobre terras raras naceu en 1794. Ese ano o químico finlandés Johann Gadolin illou o primeiro óxido da familia de terras raras. Illou o óxido dunha terra rara dun mineral obtido no municipio sueco de Ytterby. El cría que tiña un elemento novo que bautizou como iterbita. Finalmente, resumindo, chamouse itria.
Anos despois, en 1803, investigadores como Martin Heinrich Klaproth ou os famosos Jöns Jacob Berzelius, illaron á vez outra terra rara, tamén óxido. Déuselle o nome de Zeria en honra ao recentemente descuberto asteroide Zere. Isto tamén foi un elemento puro. En 1808 Sir Humphry Davy demostrou que as terras raras descubertas até entón non eran elementos, senón combinacións entre elementos metálicos e osíxeno. Aos metais que achegaban óxidos de cería e itria denomináronselles cerio e itrio.
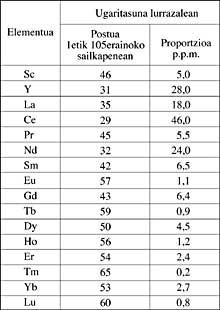
Ao longo de corenta anos considerouse que a itria e a cería, é dicir, as que se consideraban óxidos de itrio e de cerio, estaban químicamente ben definidas. Pero realmente eran mesturas de óxidos de terras raras. En 1840 o mineralogista sueco Carl Gustav Mosander logrou finalmente a división da itria e a cería en terras raras. Leste foi o descubrimento que abriu a porta ao camiño cara ao illamento de toda a sucesión de terras raras.
Nos anos posteriores realizáronse numerosas investigacións, pero dificilmente podíase avanzar. Creáronse grandes confusións ao redor de certos descubrimentos, e co fin de aclarar se estes eran elementos puros ou confusións, realizáronse numerosas publicacións. Os nomes dos elementos tamén cambiaban de laboratorio a laboratorio.
En 1869, cando o químico ruso Dimitri Ivanovitx Mendeleiev propuxo a táboa periódica, previu a necesidade de deixar un oco paira o escándo. En 1871 tamén prevé algunhas características deste elemento. Cando en 1879 descubriuse o esquandio e informouse das súas características observouse que se axustaban ao previsto por MendeleiEV. Este feito provocou que a táboa de Mendeleiev fóra aceptada entre os científicos.
As investigacións proseguiron con dureza, o que permitiu illar a lutecio en 1907, último elemento da serie.
Pero a verdade é que o elemento prometio non se illou até moito máis tarde. Cando Henry Moseley asignou a cada elemento da Táboa Periódica un número atómico, púidose coñecer exactamente onde estaban os buracos libres. Até os anos 1913-14 e Moseley descubriu que os lantánidos só podían ser 14 (desde o ceo até a lutecia) e que o número atómico 61 era o único que aínda estaba por descubrir. Con todo, non se illou até 1947. Denominóuselle Prometio.
Por que foi tan difícil identificar e illar estes elementos? A razón pode estar en que estes elementos se atopan nun mesmo mineral e presentan características químicas moi similares. Por iso estiveron escondidos durante tanto tempo. O máis lantánido é o grupo de elementos con características máis similares. Analizando un metal dado por puro nun descubrimento coas novas técnicas desenvolvidas nos próximos anos, en máis dunha ocasión púidose comprobar que era una mestura de dúas ou tres terras raras.
Una vantaxe de ter propiedades químicas tan similares é que, no uso industrial, cando se deben aproveitar estas propiedades, non merece a pena una distribución moi fina. Esta distribución resulta necesaria cando as características a aproveitar son características físicas.
Estrutura electrónica
A continuación veremos como están dispostos os electróns destes elementos. Sábese que os electróns se dispoñen en capas ao redor do núcleo do átomo. A cada capa correspóndelle un número cuántico n e paira os lantánidos n = 6. Cada capa ten un determinado número de electróns e estes están organizados á súa vez en subcapas. Estas subcapas son "s", "p", "d" e "f".
A medida que aumenta o número atómico, o número de electróns tamén aumenta. Á estrutura electrónica do elemento anterior engadiráselle un novo electrón polo que se relaciona a continuación. O electrón engadido non se situará en calquera lugar. Una serie está formada polo conxunto de elementos que corresponden ao número de electróns necesarios até completar una subcapa en formación.
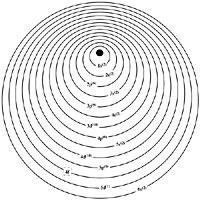
Os electróns máis estables son os electróns "s" e "p", polo que tenden a situarse nestas primeiras subcapas. Ao finalizar o quinto período da Táboa Periódica, as subcapas 4s, 4p, 4d e 5s e 5p están completas. O sexto período comeza coa incorporación de dúas 6s electróns e o terceiro vai ao orbital 5d formando o elemento denominado lantano. O cuarto electrón diríxese á subcapa 4f, até entón baleira. Dado que esta subcapa ten capacidade paira 14 electróns, a serie está composta por 14 lantánidos, desde o cero até o lutecio.
O itrio e o escandio que forman a familia das terras raras atópanse na mesma columna da táboa periódica na que se atopa o lantano. Os electróns máis superficiais do escandio son dous electróns 4s e un electrón 3d. No caso do itrio, os electróns 5s e 4d.
Primeiros usos de terras raras
O cerio foi o primeiro que gañou fama e fama entre as terras raras e que en certa medida provocou investigacións até coñecer a toda a familia.
O descubrimento realizado polo barón Auer von Welsbach en 1883 está na base do interese que suscitou o ceo. O barón publicou ese ano un novo método de iluminación. Welsbach mollaron un tecido en disolución de sales de torio, cerio e outras terras raras. A continuación descubriu que o tecido dá luz brillante póndoo en calor dunha chama de gas. Era un descubrimento moi sorprendente paira esta época. Trátase dunha característica que aínda se utiliza na actualidade, xa que é o modo de funcionamento da camisa refractaria das lámpadas de gas do cámping.
Anos despois, en 1903, o propio Auer von Welsbach descubriu outro uso de terras raras: a pedra mechera. O cerio é un piroforo, é dicir, ten a facilidade de inflamarse espontaneamente no aire e de sacar faíscas fregando. O cerio tivo que ser aleado con ferro paira usalo en pedras de chisqueiro, de maneira que non se alimentaba do lume. Este é o primeiro paso que se deu paira utilizar terras raras en metalurgia.
Una característica común a estes dous usos é que non requiren elementos de gran pureza. Por iso, puidéronse explotar industrialmente naqueles tempos nos que os métodos de distribución química paira estes usos non estaban tan desenvolvidos.
Usos industriais actuais
Metalurgia

Entre 1960 e 1974 una aliaxe denominada mischmetal, composta por lantanos, cerios e neodimios, experimentou un espectacular auxe nos procesos de fundición e purificación do aceiro. Debido á afinidade desta aliaxe co osíxeno e o xofre, é adecuada paira o seu uso como desoxidante e desulfurante. Mellora as propiedades anticorrosivas.
No ferro fundido, os materiais son máis resistentes, dúctiles e por tanto máis fáciles de procesar.
Na actualidade redúcese o uso de leste mischmetal ao aumentar o uso de compostos de calcio na desulfurización.
Reaccións catalizadas
As terras raras están moi estendidas en reaccións químicas como a polimerización ou a hidroxenación, que serven paira acelerar ou modificar. Os lantánidos raramente actúan como auténticos catalizadores, sendo o seu papel asegurar a estabilidade, activación e selectividade do sistema catalítico.
No cracking do petróleo, por exemplo, utilízanse como catalizadores estruturas cristalinas denominadas zeolitas. Están constituídos por silicio e aluminio e elementos alcalinos como potasio e sodio. A substitución do sodio por unha mestura de terras raras mellora as características catalíticas e a vida efectiva da zeolita.
Bote catalítico de vehículos
Os catalizadores utilízanse no bote catalítico paira estabilizar, optimizando o seu funcionamento e alargando a súa vida. Os potes catalíticos obtéñense mediante a aplicación de compoñentes activos (platino, paladio e rodio) nunha estrutura similar ás celas de abella formadas por aluminio e óxidos de cerio ou lantano. Nos países con lexislación anticontaminación máis esixente, o uso do bote catalítico é absolutamente necesario, o que significa que se necesitan centos de toneladas de terras raras anuais.
Vidro e cerámica
A industria do vidro e a cerámica é un dos maiores consumidores de terras raras. As terras raras absorben e emiten selectivamente varias lonxitudes de onda do espectro visible e ultravioleta. Por tanto, as cores obtidas son moi claros, moi definidos e estables. Por iso, as terras raras utilízanse como colorantes e mesmo como luminoforos.
Aínda que pareza o contrario, as terras raras tamén se utilizan paira obter vidro incoloro. Engadindo a un vidro vermello una estraña terra que absorbe selectivamente o vermello, obtense un vidro incoloro que reequilibra o espectro de cores.
Os vidros con terras raras soportan moi ben a luz solar, polo que se utilizan non só paira xanelas senón tamén paira lentes de sol.
Pantalla de TV en cor
Como xa se mencionou anteriormente, o primeiro uso industrial do óxido de cerio foi o chisqueiro de Welsbach, como din Auer, ou outros. Sabemos que o que está por baixo deste uso é una característica que se converte en luminiscente coa calor. Este resultado era extremadamente sorprendente naqueles tempos, polo que xurdiu un gran interese entre científicos e non científicos sobre terras raras. Pero foi necesario esperar até a década dos 60 paira poder dar valor a esta propiedade física.
Para entón, imos ter en conta que paira a década dos 60 os métodos de distribución química estaban moito máis desenvolvidos e apareceu una televisión de cores. Os luminoforos, é dicir, os aspectos sensibles do tubo catódico, ademais de ter una boa luminosidade e una longa duración, deben dar unha cor moi ben definida. Dado que o vanadato do itrio activado por Europa cumpre estes requisitos, utilízase en pantallas de TV en cor.
Estas son as características que xustifican o uso do europio na iluminación fluorescente.
Imáns permanentes
En 1969 os investigadores descubriron que coa introdución do samario nunha aliaxe de cobalto obtíñase un imán duradeiro extremadamente poderoso. Este imán é moi resistente á desimantación e é 30 veces máis forte que os imáns tradicionais e seis veces máis forte que as ferritas (os mellores imáns da hora).
Coas terras raras pódense conseguir imáns moito máis pequenos que teñen a mesma forza e así podemos chegar ao Walkman do ditxoso, tan coñecido na actualidade. As vantaxes que ofrecen os imáns de samario e cobalto son tan elevadas que se utilizan na maioría dos electroimanes de motores de baixa e media potencia, aínda que o seu prezo sexa moi elevado.
Co obxectivo de superar a barreira do prezo, realizáronse máis investigacións e en 1983 detectouse que os imáns compostos por ferboros e neodimios teñen as propiedades adecuadas. Desta forma pódese evitar o uso dun metal tan caro como o samario. Este novo material non mantén as súas características por encima dos 300ºC (mentres que o samario-cobalto mantenos até os 700ºC), o que dificulta o seu uso paira certas funcións como os motores de arranque de vehículos.
Por superconductividad

A superconductividad consiste na desaparición da resistencia eléctrica e por tanto da disipación enerxética. Moitos materiais presentan esta propiedade cerca do cero absoluto (-273ºC).
Nos estudos dos últimos anos atopáronse materiais que presentan esta propiedade a temperaturas superiores. En 1986, un óxido de lantano, bario e cobre foi achado como superconductor a -243ºC. A. Müller e J.G. Os físicos alemáns Bednorz. Por este traballo recibiron o Premio Nobel e abriron una nova etapa no campo da superconductividad a temperaturas máis altas.
Os novos estudos levaron o límite até -183ºC con óxidos ternarios con terras raras. Hoxe en día a marca alcanzou os -148ºC e ninguén sabe até que punto os investigadores poderán levar esta limitación nos próximos anos.
Os usos mencionados non pechan a lista. A radioloxía, os láseres, a óptica de axuste e a xoiaría son campos que aproveitan as propiedades das terras raras.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian