Sumando forzas na loita contra o cancro de fígado
Segundo a mitoloxía grega, Prometeo roubou o lume do monte Olinpo e entregouno aos humanos. Entón, Zeus castígao, atouno nunha roca e durante unha tempada enviou un aguia a comer todas as noites os anacos do seu fígado. Con todo, á mañá seguinte, cada vez, Prometeo recuperábase do fígado, pero pola noite a aguia volvía a masacre no ventre. Así paira sempre. Moitas veces díxose que o fígado de Prometeo representa á vez a fortaleza e a debilidade do ser humano, destruído cada noite e creado cada mañá.
Esta pasaxe demostra que desde a antigüidade coñécese o carácter especial e a importancia do fígado. E é que o fígado é un dos órganos máis importantes do ser humano e, en xeral, dos animais vertebrados. Así, o cancro provoca unha chea de mortes ao atacar o fígado, o segundo dos máis letais [1]. Ademais, entre un 60% e un 80% dos pacientes con cancro de colon, páncreas ou mama padecen metástasis hepáticas, é dicir, os tumores xerados fóra do fígado esténdense ao fígado [2]. É evidente, por tanto, que as investigacións sobre o cancro de fígado son moi importantes. Grazas a eles chegaron tratamentos como a denominada radioembolización. Nos últimos anos esta última está a imporse.
Nas seguintes liñas explicaranse as achegas de interese que poden facer os enxeñeiros industriais á radioembolización e ao medicamento en xeral. Paira afrontar novos retos cada vez máis complexos é necesario que profesionais de diferentes ámbitos traballen na mesma dirección, en colaboración. O autor colaborou cos médicos da Clínica Universidade de Navarra. En concreto, durante a súa tese doutoral ha analizado a radioembolización e diversas variables que poden influír no tratamento.
Radioembolización
A embolización consiste en obstruir (pechar) os vasos sanguíneos, en definitiva impedir o transporte do sangue. A irradiación é o uso terapéutico da enerxía radioactiva.
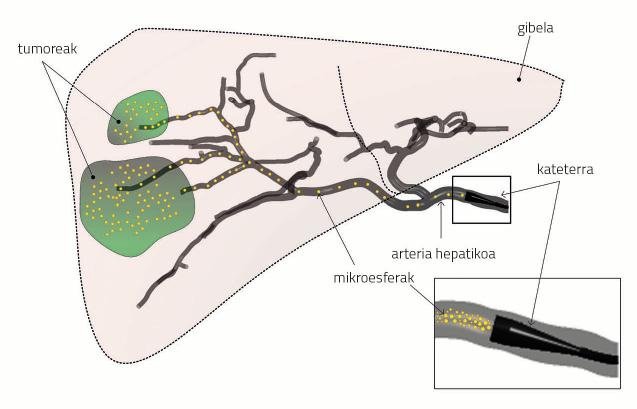
Durante a radioembolización, o médico realiza una incisión na arteria femoral (zona inguinal), onde introduce un catéter de diámetro aproximado 1 mm. Despois lévao manualmente até a arteria hepática (arteria hepática). Una vez situado o extremo do catéter na arteria hepática inxecta microesferas radioactivas de 32 ?m de diámetro (e presentes na auga). O fluxo sanguíneo transporta as microesferas. O obxectivo é transferir as partículas radioactivas aos tumores e minimizar a irradiación das partes sas do fígado (ver figura 1).
As microesferas levan adherido un radioisótopo itrio-90 (emite irradiación beta ao redor de 2,5 mm de retorno, cunha vida media de 2,6 días). O tratamento dura aproximadamente una hora e normalmente o paciente volve a casa o mesmo día.
Con todo, antes de jeringar as microesferas que constitúen una fonte de radiación no corpo, é necesario un tratamento previo que asegure a chegada das partículas ao lugar adecuado. O pretratamiento realízase con partículas inocuas. Así, mediante imaxes médicas analízase o destino das microesferas. Este estudo serve paira determinar a posición do catéter no tratamento (sensu estrito) e a velocidade coa que se inxectan as microesferas.
O tratamento é seguro e efectivo. Con todo, hai que ter en conta que o médico coloca o catéter de forma manual e recita microesferas a man. Por tanto, se a localización do catéter e a velocidade de inxección de partículas non son exactas, e por tanto irrádianse zonas que non deben ser tratadas, poden xurdir problemas como hepatites, pneumonía e úlceras estomacais e intestinais.
Enxeñeiros sumando o exército da radioembolización
A radioembolización é un tratamento realmente complexo, xa que require a colaboración dos intervencionistas de radioloxía, oncólogos de radiación, médicos nucleares, etc. (físicos médicos, hepatólogos, etc.). Na citada tese, os enxeñeiros uníronse a este gran grupo co obxectivo de analizar a dinámica do fluxo sanguíneo na arteria hepática e o comportamento das súas partículas.
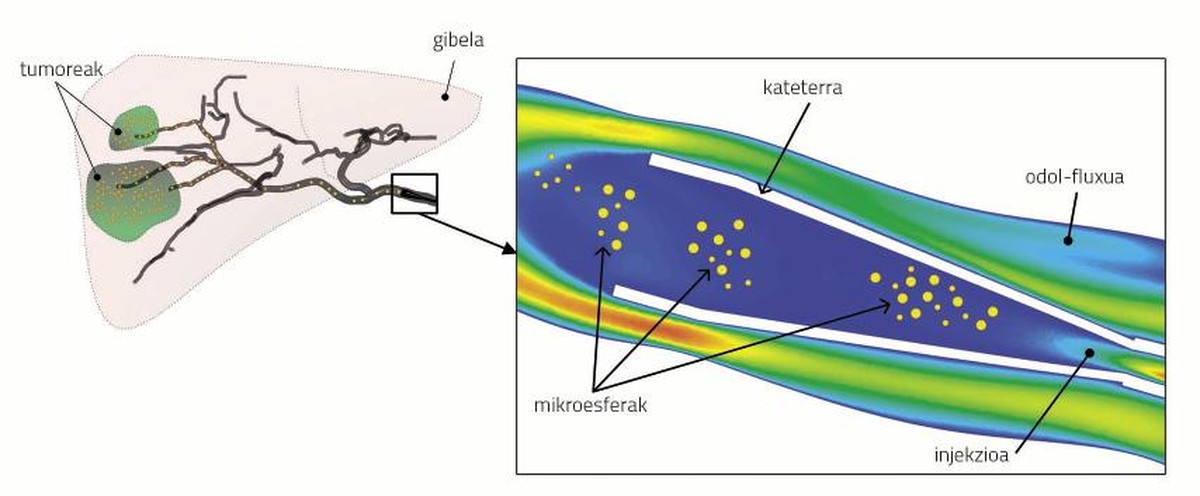
Durante o estudo utilizouse a ferramenta Computational Fluíde Dynamics (CFD) paira simular o fluxo sanguíneo e o transporte de microesferas. O CFD considera a xeometría, as ecuacións do fenómeno físico e as condicións límite. A xeometría consiste en definir en que zonas estudarase o fluxo sanguíneo e o transporte de microesferas. Pola contra, as ecuacións do fenómeno físico definen o fluxo sanguíneo e o transporte das microesferas. Por último, o establecemento das condicións límite implica a colocación de determinadas características nos límites da zona obxecto de estudo, tanto no que se refire ao fluxo sanguíneo (presión e velocidade) como ás microesferas (velocidade).
Una adecuada definición do tres compoñentes permite elaborar un modelo fiable. E, por suposto, as simulacións realizadas cun modelo fiable representan a presión e velocidade do sangue e a velocidade das partículas. Na figura 2 pódese observar, por exemplo, a velocidade do fluxo sanguíneo ao redor do catéter e a localización das microesferas.
Pero hai que ter claro que na análise só se pode analizar o que ocorre na primeira parte do transporte. De momento, non é posible ver como viaxan as microesferas a través de pequenas arterias, nin o efecto da irradiación no tumor. Por iso, na investigación, diremos que a radioembolización é un éxito se as microesferas salguen das saídas esperadas, é dicir, dos condutos que fornecen sangue aos tumores (Figura 1).
Parámetros analizados
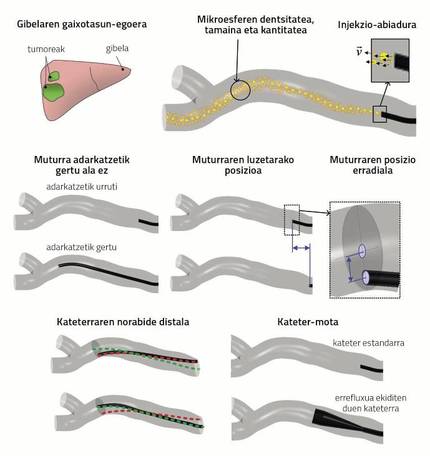
A investigación baseada en simulacións CFD realizouse co obxectivo de dar resposta ás fontes de discusión atopadas na literatura e ás inquietudes dos médicos da Clínica Universidade de Navarra. Paira iso seleccionáronse una serie de parámetros que parecían influír no resultado da radioembolización. A figura 3 pode axudar a comprender os parámetros que se enumeran a continuación, xa que resume gráficamente as variables.
? Estado de enfermidade do fígado: relacionado co tamaño, localización e tipo dos tumores. Afecta á demanda sanguínea do fígado e, por tanto, á capacidade de tomar microesferas.
? Densidade, tamaño e cantidade das microsferas: as microesferas utilizadas en pretratamiento e tratamento son diferentes.
? Velocidade de inxección de microsferas: é difícil reproducir en tratamento este parámetro especificado no pretratamiento, xa que, como xa se indicou, o médico inxecta as partículas manualmente.
? Proximidade da punta do catéter á bifurcación do vaso sanguíneo.
? Posición longitudinal do extremo: aquí tamén é difícil repetir en tratamento o especificado no pretratamiento.
? Posición radial do extremo: outro tanto.
? Dirección distal do catéter: o mesmo.
? Tipo de catéter: na actualidade existen numerosas investigacións sobre o deseño en marcha. Na investigación á que se refire este artigo estudouse o catéter estándar e o catéter que evita o reflujo (véxase o “Tipo de catéter” da figura 3).
Non hai que esquecer que a modificación dalgún parámetro modifica a distribución das microesferas e o seu destino. Ademais, a colocación dun catéter na arteria supón a modificación das características hemodinámicas (presión e velocidade) do fluxo sanguíneo, que ao ser una barreira física condiciona o fluxo natural. Como consecuencia, a traxectoria e distribución das microsferas varía. Por iso, é moi importante coñecer de antemán as características do fluxo sanguíneo próximo ao extremo do catéter.
Aínda que na tese analizouse a influencia de cada un dos oito parámetros da lista, aquí explicarase a situación do catéter, probablemente a variable máis importante.
Importancia da localización do catéter
Ao facer o corte e introducir o catéter hai dúas opcións principais: que o extremo do catéter quede preto dalgunha das ramificacións da arteria ou que quede afastado (ver “extremo próximo ou non á ramificación” da figura 3). O resto de parámetros relacionados coa localización do catéter son a posición longitudinal do extremo, a posición radial do extremo, a dirección distal do catéter e o tipo de catéter (ver figura 3).
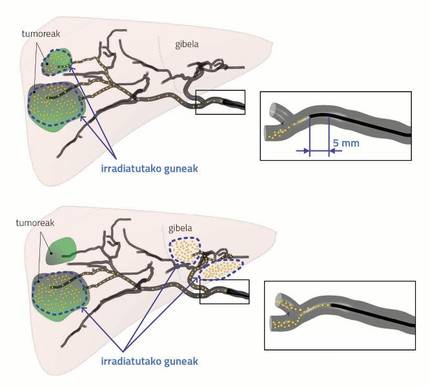
Se a inxección realízase lonxe da bifurcación, a distribución das microesferas adopta a forma de fluxo sanguíneo, aliñándoas co fluxo sanguíneo. Neste caso, os cambios no resto de parámetros non afectan á distribución das microsferas. Con todo, se as partículas se xiringen preto da bifurcación, os cambios nos parámetros condicionan a distribución das microesferas.
A figura 4 mostra claramente que una diferenza de pouco máis de 5 mm (lonxitude dunha formiga) ten una gran influencia na distribución das partículas. A xiringación próxima (caso superior) é o resultado dunha exitosa radioembolización que consiste en transferir as microesferas a ambos os tumores (irradiación de ambos os tumores). Lonxe, con todo, non. No segundo caso, uno dos tumores non foi irradiado e, ademais, o fígado san foi bombardeado.
Reflexións finais
O que está claro desde a época de Prometeo ou desde antes é que a saúde é a principal responsabilidade humana.
Ademais, os enxeñeiros Sznitman e Steinman previron que as investigacións co CFD serán importantes nos próximos anos [3]. Servirán paira crear novos tratamentos ou mellorar os existentes, coidado cos enfermos de cancro!
Hai moito que facer, pero convén ir paso a paso, “rápido e ben, as pombas voando”.
Referencias
Traballo presentado aos premios CAF-Elhuyar.
Buletina
Bidali zure helbide elektronikoa eta jaso asteroko buletina zure sarrera-ontzian